煤气是生活中常用的燃料,制取水煤气的反应为C(s)+H2O(g)?CO(g)+H2(g).该反应在一容积可变的密闭容器中进行时,改变下列条件会对反应速率产生影响的是( )
①增加少量的碳 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大 ④保持压强不变,充入N2使体系体积增大.
①增加少量的碳 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大 ④保持压强不变,充入N2使体系体积增大.
| A、①② | B、②③ | C、②④ | D、①④ |
已知下列热化学方程式:
(1)H2(g)+
O2(g)═H2O(g);△H1=a kJ/mol
(2)2H2(g)+O2(g)═2H2O(g);△H2=b kJ/mol
(3)H2(g)+
O2(g)═H2O(l);△H3=c kJ/mol
(4)2H2(g)+O2(g)═2H2O(l);△H4=d kJ/mol
下列关系式正确的是( )
(1)H2(g)+
| 1 |
| 2 |
(2)2H2(g)+O2(g)═2H2O(g);△H2=b kJ/mol
(3)H2(g)+
| 1 |
| 2 |
(4)2H2(g)+O2(g)═2H2O(l);△H4=d kJ/mol
下列关系式正确的是( )
| A、a<c<0 |
| B、b>d>0 |
| C、2c=b>0 |
| D、2c=d<0 |
下列各项中表达正确的是( )
| A、硫离子的核外电子排布式:1s22s22p63s23p6 |
| B、N2的结构式::N≡N: |
C、NaCl的电子式: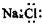 |
D、CO2的分子模型示意图: |
下列电子式书写正确的是( )
①氧原子 ②过氧根离子
②过氧根离子 ③氢氧根离子
③氢氧根离子
④钠离子[Na]+⑤氢离子H+⑥铵根离子 ⑦铝原子
⑦铝原子 ⑧
⑧
①氧原子
 ②过氧根离子
②过氧根离子 ③氢氧根离子
③氢氧根离子
④钠离子[Na]+⑤氢离子H+⑥铵根离子
 ⑦铝原子
⑦铝原子 ⑧
⑧
| A、①②③⑥⑦ |
| B、①③④⑥⑦⑧ |
| C、①③⑤⑥⑦⑧ |
| D、②③④⑦⑧ |
下列说法中不正确的是( )
| A、需要加热才能发生的反应一定是吸热反应 |
| B、化学键的断裂与形成是化学反应中能量变化的主要原因 |
| C、能量变化是化学反应的基本特征之一 |
| D、化学反应的能量变化通常表现为热量变化 |
下列说法不正确的是( )
| A、二氯甲烷、溴已烷、盐酸甘氨酸都是共价化合物 |
| B、酚醛树脂、聚乙烯、天然橡胶都是由高分子化合物组成的物质 |
| C、有机物均含有C元素,但不是所有有机物均能发生燃烧反应 |
| D、水溶液的PH不同,氨基酸在水溶液中存在形式不同,可以调节PH分离氨基酸 |
现给你提供以下试剂:①蒸馏水;②铁粉;③浓硫酸;④浓盐酸;⑤烧碱;⑥浓氨水;⑦Cl2.请你设计一个实验:从电子工业上用FeCl3溶液腐蚀印刷电路板后的废液中(含有FeCl3、FeCl2、CuCl2),回收并制取纯净的FeCl3溶液.在方案中需选用上述试剂中的( )
| A、①②④⑦ | B、①③④⑥ |
| C、②④⑥⑦ | D、①④⑥⑦ |
将标准状况下a L HCl(g)溶于100g水中,得到的盐酸的密度为b g?cm-3,则该盐酸的物质的量浓度是( )
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
 已知一定条件下:C(石墨)=C(金刚石),在该过程中其能量变化如图所示,有关该反应的描述正确的是( )
已知一定条件下:C(石墨)=C(金刚石),在该过程中其能量变化如图所示,有关该反应的描述正确的是( )| A、该过程为氧化还原反应 |
| B、金刚石和石墨互为同位素 |
| C、该反应过程是放热反应 |
| D、该反应是热能转化为化学能 |
下列实验操作正确的是( )
| A、用分液漏斗分离环己烷和苯的混合液体 |
| B、溴乙烷10%的烧碱溶液中,加热片刻后,冷却,先加过量的硝酸,再滴加2滴2%的硝酸银溶液,以检验水解生成的溴离子 |
| C、做银镜反应实验时应将醛溶液和新制备的银氨溶液混合后充分加热至沸腾 |
| D、实验室制溴苯时选用的试剂是浓溴水、苯和铁屑 |