NA设为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、标准状况下,22.4L 水中所含原子总数数为3 NA |
| B、23g钠与一定量的氧气作用,若两者均无剩余,转移NA个电子 |
| C、28.6g Na2CO3?10H2O(M=286)晶体溶于水,所得溶液中CO32-个数为0.1NA |
| D、常温下,1L 0.1mol?L-1的NH4NO3溶液中氧原子数为0.3NA |
下列说法正确的是( )
| A、电解饱和食盐水时,阳极析出氢气 |
| B、在船身装上锌块利用的是牺牲阳极的阴极保护法 |
| C、钢铁发生吸氧腐蚀负极的电极反应式是2H2O+O2+4e-=4OH- |
| D、电解精炼铜时,杂质Fe、Zn、Ag等沉积在电解槽底部 |
下列说法正确的是( )
| A、1mol H2SO4 的物质的量是98g/mol |
| B、H2SO4 的摩尔质量为98 |
| C、0.5mol的氧 |
| D、6.02×1022个 H2SO4 分子的质量为9.8g |
下列溶液中微粒浓度关系一定正确的是( )
| A、均为0.10mol?L-1 NH4Cl和NH4HSO4溶液,c(NH4+)前者小于后者 |
| B、25℃时NH4Cl溶液的KW大于100℃时NH4Cl溶液的KW |
| C、25℃时pH=11的NaOH和pH=11的氨水分别稀释100倍后的pH前者一定大于后者 |
| D、25℃时,pH=4的盐酸与pH=10的氨水溶液等体积混合后pH<7 |
服药(片剂)时,应选用下列哪种物质送服( )
| A、白开水 | B、茶水 | C、白酒 | D、汽水 |
表中原子化热、晶格能、键能的单位都是kJ?mol-1
则下列说法正确的是( )
| 金属 | 金属原子化热 | 离子化合物 | 晶格能 | 共价键 | 键能 |
| Na | 108.4 | NaCl | 786 | Cl-Cl | 243 |
| Mg | 146.4 | NaBr | 747 | Si-Si | 176 |
| Al | 326.4 | MgO | 3791 | Si-Cl | 360 |
| A、Na(s)与Cl2(g)反应生成1mol NaCl(s)放出的热量为556.1kJ |
| B、Si(s)+2Cl2(g)═SiCl4(g)△H=-602kJ?mol-1 |
| C、从表中可以看出,氯化钠的熔点比晶体硅高 |
| D、从表中数据可以看出,微粒半径越大金属键、离子键的越弱,而共价键却越强 |
 一定质量的Na.K分别投入一定量的稀盐酸中,在相同条件下产生氢气的体积随时间变化的曲线如图中a.b所示,则下列说法中正确的是( )
一定质量的Na.K分别投入一定量的稀盐酸中,在相同条件下产生氢气的体积随时间变化的曲线如图中a.b所示,则下列说法中正确的是( )| A、投入的Na.K物质的质量一定相等 |
| B、曲线a对应的反应使用了催化剂 |
| C、曲线a代表K的反应,曲线b代表Na |
| D、两反应中盐酸必须是足量的 |
把氯气通入下列各物质的溶液中,阴离子和阳离子都能被氧化的是( )
| A、NaOH |
| B、Na2SO3 |
| C、FeBr2 |
| D、FeSO4 |
设NA表示阿伏加德罗常数.下列说法中,不正确的是( )
| A、标准状况下,22.4 L氢气和氯气的混合气体,所含分子数为NA |
| B、1mol?L-1 NaCl溶液含有NA个Na+ |
| C、1mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA |
| D、1mol Na2O2中含有的阴离子数目为NA |
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
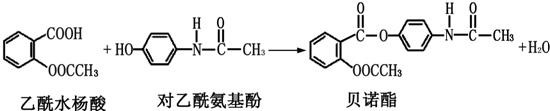
有关上述反应物和产物的叙述正确的是( )

有关上述反应物和产物的叙述正确的是( )
| A、上述反应类型为取代反应 |
| B、按碳的骨架分类,上述三种有机物均属于芳香烃 |
| C、1mol乙酰水杨酸最多能与含2mol NaOH的水溶液发生反应 |
| D、贝诺酯分子中有三种不同类型的含氧官能团 |