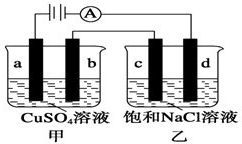
 如图a、b、c、d均为石墨电极,通电进行电解(电解液足量).下列说法不正确的是( )
如图a、b、c、d均为石墨电极,通电进行电解(电解液足量).下列说法不正确的是( )| A、甲中a的电极反应式为4OH--4e-═O2↑+2H2O |
| B、向乙中加入适量盐酸,溶液组成可以恢复 |
| C、电解时向乙中滴入酚酞溶液,d电极附近先变红 |
| D、当b极有6.4g Cu析出时,c电极产生7.1g气体 |
下列除去杂质的操作方法不正确的是( )
| A、除去SiO2中的少量NH4Cl:在空气中充分灼烧 |
| B、除去CO2中混有的SO2:用NaOH溶液洗气,再干燥 |
| C、除去铜器表面的铜绿【Cu2(OH)2CO3】:用盐酸浸泡,再用清水冲洗 |
| D、除去苯中溶解的Br2:加入足量NaOH溶液,充分振荡后,静置分液 |
某氧化还原反应:A(g)+B(g)?2C(g)+D(s)△H<0,反应达到平衡后,在其他条件不变的情况下,下列说法正确的是( )
| A、加入催化剂,改变了反应的途径,反应的△H也随之改变 |
| B、改变压强,平衡不发生移动,反应放出的热量不变 |
| C、升高温度,反应速率加快,反应放出的热量不变 |
| D、若该反应在原电池中发生,达到平衡后测得放出的热量在数值上与△H相同 |
一定量的SO2和NaOH溶液反应,所得产物中含有Na2SO3和NaHSO3物质的量之比为3:5,则参加反应的SO2和NaOH的物质的量之比为( )
| A、8:11 | B、3:5 |
| C、1:2 | D、18:8 |
已知反应A+B=C+D的能量变化如图所示,下列关于此反应的说法不正确的是( )
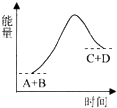

| A、是吸热反应 |
| B、只有在加热条件下才能进行 |
| C、生成物的总能量高于反应物的总能量 |
| D、反应中断开化学键吸收的总能量高于形成化学键放出的总能量 |
VmL硫酸铁溶液中含a g Fe3+,从该溶液中取出
mL,并稀释至2VmL,则稀释后溶液中的SO42-物质的量浓度约为( )
| V |
| 2 |
A、
| ||
B、
| ||
C、
| ||
D、
|
原电池发生的反应是可自发进行的氧化还原反应,CO/O2燃料电池以熔融状态的碳酸盐为电解质,下列说法正确的是( )
| A、CO在正极通入 |
| B、CO32-在电池内部向正极移动 |
| C、当有22.4LCO参加反应时电路中有2mol电子发生转移 |
| D、该电池电解质在固态时,电池无法工作 |
下列说法正确的是( )
| A、向Na2CO3溶液中滴入酚酞后溶液变成红色,说明Na2CO3溶液具有碱性,属于碱 |
| B、将SO2通入氯水中,溶液颜色退去,说明SO2具有漂白性 |
| C、制备无水AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 |
| D、Fe与稀硝酸、稀硫酸反应均有气泡冒出,说明Fe与两种酸均发生了置换反应 |
在指定条件的下列溶液中,一定能大量共存的微位是( )
| A、0.1mol/L的CH3CHO的溶液中:MnO4-、SO42-、H+、K+ | ||
| B、pH=2的CH3COOH的溶液中:Fe3+、Na+、C6H5O-、SO42- | ||
C、
| ||
| D、pH=6的NH4Cl溶液中:CO32-、K+、Na+、NO3- |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、1.0mol?L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B、甲基橙呈红色的溶液:NH4+、Ba2+、CH3COO-、Cl- |
| C、pH=12的溶液:K+、Na+、ClO-、NO3- |
| D、含有0.1mol/LCa2+的溶液中:Na+、K+、CO32-、NO3- |