下列反应方程式中正确的是( )
| A、碳酸钠的水解方程式:2H2O+CO32-?H2CO3+2OH- | ||
| B、用盐酸溶解碳酸钙的离子方程式:2H++CaCO3=H2O+Ca2++CO2↑ | ||
C、甲醇的燃烧热的热化学方程式:CH3OH(l)+
| ||
| D、CaCO3的电离方程式:CaCO3?Ca2++CO32- |
原电池中发生的反应一定是( )
| A、化合反应 |
| B、置换反应 |
| C、非氧化还原反应 |
| D、氧化还原反应 |
下列推断合理的是( )
| A、金刚石是自然界中硬度最大的物质,不可能与氧气发生反应 |
| B、将SO2分别通人品红和氯水溶液,溶液都会褪色,而且再经加热都能恢复原色 |
| C、浓H2SO4,具有强氧化性,不能与Cu发生剧烈反应 |
| D、明矾[KAl(SO4)2?12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
下列叙述正确的是( )
| A、摩尔是指物质所含的粒子个数,它是物质的数量单位 |
| B、阿伏加德罗常数通常用NA表示,6.02×1023mol称为阿伏加德罗常数 |
| C、氦气的摩尔质量是8g |
| D、4.4g二氧化碳气体中所含的原子个数与4.2g氮气中所含的原子个数相等 |
下列离子方程式书写正确的是( )
| A、盐酸滴人氨水中:H++OH-═H2O | ||
B、过量的SO2通人NaOH溶液中:SO2+20H-=SO
| ||
| C、Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++2H2O | ||
| D、硫酸亚铁溶液与稀硫酸、双氧水混合:2Fe2++H2O2+2H+=2Fe3++2H2O |
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
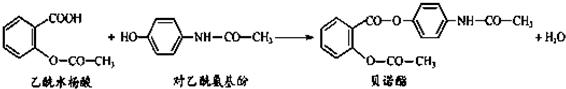
下列有关叙述正确的是( )

下列有关叙述正确的是( )
| A、贝诺酯分子中有三种含氧官能团 |
| B、对乙酰氨基酚核磁共振氢谱中共有四个峰 |
| C、乙酰水杨酸和对乙酰氨基酚均能与Na2CO3 溶液反应 |
| D、贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠 |
下列关于中和热的说法中正确的是( )
| A、10 L 0.05 mol?L-1Ba(OH)2溶液与20 L 0.05 mol?L-1 HNO3反应时的反应热是中和热 |
| B、1 mol HCl气体通入1 L 0.01 mol?L-1 NaOH溶液中反应时的反应热是中和热 |
| C、1 mol HClO与2 mol NaOH溶液反应时的反应热也可能是中和热 |
| D、只要强酸与强碱在稀溶液中反应生成1 mol水时的反应热就是中和热 |
在无色强酸性溶液中可能大量共存的离子组是( )
| A、Ba2+、NH4+、S2-、MnO4- |
| B、NH4+、Na+、Br-、Cl- |
| C、K+、Ca2+、HSO3-、NO3- |
| D、Fe2+、NH4+、Cl-、SO32- |
下列各组离子,在指定的环境中一定能大量共存的是( )
| A、在pH为7的溶液中:Ag+、K+、SO42-、Cl- |
| B、在能使pH试纸变深蓝色的溶液中:Na+、S2-、NO3-、CO32- |
| C、在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3- |
| D、在由水电离出的c(OH-)=10-13mol?L-1的溶液中:Na+、Mg2+、Cl-、I- |
常温下,在等体积①pH=3的醋酸、②0.005mol/L Ba(OH)2溶液、③pH=10的纯碱溶液、④pH=5的NH4Cl溶液中,水电离程度的大小顺序是( )
| A、②>①>④>③ |
| B、③>④>①>② |
| C、③>④>②>① |
| D、④>③>①>② |