设NA为阿伏加德罗常数的值,下列对0.3mol?L-1的K2SO4溶液说法不正确的是( )
| A、1L溶液中含有K+和SO42-总数为0.9NA |
| B、1L溶液中含有K+的数目为0.6NA |
| C、2L溶液中含有SO42-的数目为0.6NA |
| D、2L溶液中K+物质的量浓度为1.2 mol?L-1 |
在标准状况下,1L氧气约含有n个分子,则阿伏加德罗常数的值可表示为( )
| A、n/22.4 | B、n/32 |
| C、n/16 | D、22.4n |
对1mol H2O的说法正确的是( )
| A、含有6.02×1023个氢分子 |
| B、含有6.02×2×1023个氢元素 |
| C、质量为18g |
| D、氢原子与氧原子的质量之比为2:1 |
100℃时,下列各溶液中,离子的物质的量浓度关系正确的是( )
| A、0.1mol/L的醋酸溶液中C(H+)=1×10-1mol/L |
| B、小苏打溶液中:C(Na+)=C(HCO3-) |
| C、KCl溶液中:C(H+)+C(K+)=C(0H-)+C(Cl-) |
| D、PH=12的KOH溶液中:C(OH-)=1×10-2mol/L |
在甲烷与氯气发生取代反应的产物中,室温下呈气态的有机物有( )
| A、一种 | B、两种 | C、三种 | D、四种 |
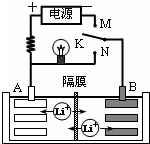 如图是一种可充电的锂离子电池充放电的工作示意图.放电时该电池的电极反应式为:负极:LixC6-xe-=C6+xLi+(LixC6表示锂原子嵌入石墨形成的复合材料)正极:Li1-xMnO2+xLi++xe-=LiMnO2(LiMnO2表示含锂原子的二氧化锰).下列有关说法正确的是( )
如图是一种可充电的锂离子电池充放电的工作示意图.放电时该电池的电极反应式为:负极:LixC6-xe-=C6+xLi+(LixC6表示锂原子嵌入石墨形成的复合材料)正极:Li1-xMnO2+xLi++xe-=LiMnO2(LiMnO2表示含锂原子的二氧化锰).下列有关说法正确的是( )| A、在整个充、放电过程中至少存在3种形式的能量转化 | |||
| B、K与M相接时,A是阴极,发生还原反应 | |||
| C、K与N相接时,Li+由A极区迁移到B极区 | |||
D、该电池的总反应式为Li1-xMnO2+LixC6
|
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、22.4 L 氢气中含有氢分子数目为NA | ||
| B、0.5mol Na2CO3中含有的Na+数目为 0.5 NA | ||
| C、常温常压下,14 g 氮气含有的原子数目为 NA | ||
D、0.5 mol/L Fe2(SO4)3溶液中,S
|
在一定温度下,将等物质的量的CO和水蒸气通入恒容密闭容器中,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),一段时间后反应达到平衡.对该平衡状态描述正确的是( )
| A、正反应速率等于零 |
| B、各组分的浓度保持一定 |
| C、反应已经停止 |
| D、正反应速率小于逆反应速率 |
已知,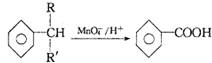 ,某分子式为C11H16的含一个苯环的有机物,其被酸性高锰酸钾溶液氧化得到
,某分子式为C11H16的含一个苯环的有机物,其被酸性高锰酸钾溶液氧化得到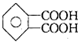 ,则该有机物可能的结构有( )
,则该有机物可能的结构有( )
 ,某分子式为C11H16的含一个苯环的有机物,其被酸性高锰酸钾溶液氧化得到
,某分子式为C11H16的含一个苯环的有机物,其被酸性高锰酸钾溶液氧化得到 ,则该有机物可能的结构有( )
,则该有机物可能的结构有( )| A、2种 | B、3种 | C、4种 | D、5种 |
加热KMnO4,收集到aL氧气(标准状况),反应中转移的电子数为b mol,则标准状况的气体摩尔体积Vm(L/mol)可以表示为( )
A、
| ||
B、
| ||
C、
| ||
D、
|