如图所示的实验方法、装置或操作完全正确的是( )
A、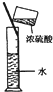 稀释浓H2SO4 |
B、 萃取时振荡 |
C、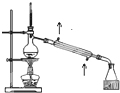 石油的蒸馏 |
D、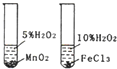 研究不同催化剂对反应速率的影响 |
下列分离物质的方法中,根据微粒大小进行分离的是( )
| A、萃取 | B、重结晶 | C、聚沉 | D、渗析 |
下列的排序不正确的是( )
| A、晶体熔点由低到高:CF4<CCl4<CBr4<CI4 |
| B、沸点由高到低:Na>Mg>Al |
| C、硬度由大到小:金刚石>SiC>晶体硅 |
| D、晶格能由大到小:MgF2>NaCl>NaBr |
白钨矿(主要成分为CaWO4)是一种重要的含钨矿物,CaWO4中钨元素(W)的化合价是( )
| A、+6 | B、+4 | C、+2 | D、-2 |
在标准状况下①2.24L CH4 ②3.01×1023个HCl分子 ③0.2mol NH3,下列对这四种气体的关系从大到小表达不正确的是( )
| A、体积②>③>① |
| B、物质的量 ②>③>① |
| C、质量③>②>① |
| D、氢原子个数③>②>① |
下列离子方程式正确的是( )
| A、大理石与盐酸反应:CO32-+2H+=H2O+CO2↑ |
| B、钠与硫酸铜溶液反应:Cu2++2Na=2Na++Cu |
| C、铁与稀硫酸的反应:Fe+2H+=Fe2++H2↑ |
| D、Ba(OH)2溶液与H2SO4溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
某温度下氯气和氢氧化钠溶液反应,生成NaClO、NaClO3、NaCl、H2O.且NaClO、NaClO3物质的量之比为1:3,则被氧化的氯原子和被还原的氯原子的物质的量之比为( )
| A、1:1 | B、4:1 |
| C、5:1 | D、1:4 |
一定温度下,Na2CO3溶液中存在水解平衡:CO32-+H2O?HCO3-+OH-.下列说法中,正确的是( )
A、升高温度,
| ||||||
| B、通入CO2,平衡向正反应方向移动 | ||||||
| C、稀释溶液,Na2CO3水解程度增大,水解平衡常数增大 | ||||||
| D、加入NaOH固体,平衡向逆反应方向移动,溶液pH减小 |
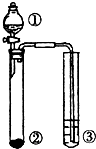 利用图示实验装置,能达到实验目标的是( )
利用图示实验装置,能达到实验目标的是( )