T℃时,将NO2和N2O4的混合气体通入容积不变的密闭容器中,发生反应:2NO2(g)?N2O4(g)△H<0.各组分的浓度随时间的变化如图.下列说法正确的是( )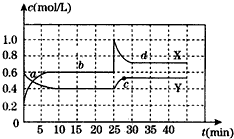

| A、第35min时,NO2的体积分数高于第15min时的体积分数 |
| B、T℃时,N2O4(g)?2NO2(g)的平衡常数为0.9 |
| C、a、b、C、d四点中,气体颜色最浅的是C点 |
| D、0~10min内反应体系对外界放热,25~30min内反应体系从外界吸热 |
已知有如下反应:Cl2+2I-=2Cl-+I2;Cl2+2Fe2+=2Cl-+2Fe3+;2Fe3++2I-=I2+2Fe2+;I2+SO2+2H2O=2I-+SO42-+4H+,下列叙述正确的是( )
| A、该反应是不可能发生的:Cl2+SO2+2H2O=2Cl-+SO42-+4H+ |
| B、氧化性:Cl2>Fe3+>I2 |
| C、还原性:I->Cl->Fe2+ |
| D、将SO2通入FeCl3溶液中得不到 SO42- |
25℃时,用0.1mol/L的醋酸溶液做了以下实验,不能证明其为弱酸的是( )
| A、pH大于1 |
| B、溶液中含有HAc分子 |
| C、溶液中含有OH- |
| D、导电能力比0.1mol/L的盐酸弱 |
下列离子方程式中,不正确的是( )
| A、KI的酸性溶液长期置于空气中:4I-+4H++O2═2I2+2H2O |
| B、高锰酸钾酸性溶液与草酸溶液反应:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O |
| C、用稀硫酸除去铁片表面的铁锈:FeO+2H+═Fe2++H2O |
| D、硫代硫酸钠溶液中滴加稀硫酸:2H++S2O32-═S↓+SO2↑+H2O |
下列变化必须加入氧化剂才能实现的是( )
| A、CuO→Cu |
| B、Fe→FeCl2 |
| C、HNO3→NO2 |
| D、Al2O3→NaAlO2 |
SiCl4的分子结构与CCl4类似,对其作出如下推断:①常温常压下SiCl4是分子晶体;②常温常压下SiCl4是液体;③SiCl4是由共价键形成的分子;④SiCl4熔点高于CCl4.其中正确的是( )
| A、只有①②④ | B、只有①②③ |
| C、只有②③④ | D、①②③④ |
下列各组物质都是还原剂的是( )
| A、H+、S、K+、Cl2 |
| B、Fe2+、Zn、S2-、C |
| C、Fe3+、I-、H2、CO |
| D、Al、Zn2+、Na、I- |
除去苯中所含的苯酚,可采用的适宜方法是( )
| A、加足量NaOH溶液,分液 |
| B、加适量 浓溴水,过滤 |
| C、加70℃以上的热水,分液 |
| D、加适量FeCl3溶液,过滤 |
天然气根据成分不同分为贫气和富气,贫气中甲烷的含量较多,富气中乙烷、丙烷、丁烷的含量相对高一些.若要将它们液化,下列说法正确的是( )
| A、贫气易液化 |
| B、富气易液化 |
| C、二者液化条件相同 |
| D、加压降温均有利于两者液化 |
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | NaCl(Na2CO3) | 盐酸 | - |
| B | CO2(CO) | O2 | 点燃 |
| C | Fe(Cu) | 稀硫酸 | 过滤 |
| D | CO2(HCl) | NaOH溶液 | 洗气 |
| A、A | B、B | C、C | D、D |