下列说法正确的是( )
| A、一定温度下,将盐酸滴加入醋酸钠溶液中至呈中性.此时溶液中:c(Na+)>c(Cl-)=c(CH3COOH) |
| B、常温下,将0.1 mol?L-1氨水稀释10倍后,其pH大于12 |
| C、常温下,Ksp(CaCO3)=2.8×10-9,Ksp(CaSO4)=4.9×10-5,则反应CaSO4(s)+CO32- (aq)═CaCO3(s)+SO42-(aq) 平衡常数K约为1.75×10-4 |
| D、溶有等物质的量的NaClO、NaHCO3的混合溶液中:c(HClO)+c(ClO-)=c(CO32-)+c(HCO3-)+c(H2CO3) |
将下列物质按酸、碱、盐分类排列,正确的是( )
| A、硫酸、纯碱、CaSO4 |
| B、HCl、烧碱、CuSO4 |
| C、HNO3、乙醇、氯化钠 |
| D、碳酸、CaO、苛性钠 |
X、Y、Z、W 是原子序数依次递增的四种短周期元素,甲、乙、丙、丁是它们两两组合而成的化合物,且能发生甲+乙=丙+丁的反应,乙、丙、丁的化学式分别为Y2Z、YW2、ZX4,丁的结构类似甲烷,0.1 mol?L-1 甲的水溶液pH 为1(25℃).下列说法正确的是( )
| A、原子半径:W>Z>Y>X |
| B、Y 元素在周期表中的位置为第三周期第ⅡA 族 |
| C、丁的稳定性大于甲烷 |
| D、0.1 mol?L-1 甲的水溶液中,由水电离产生的c(H+)=0.1 mol?L-1 |
锂空气电池优点很多,有望替代传统锂电池技术,工作原理如下:如图1电池中的固体电解质隔膜只有锂离子穿过.请仔细看图2,在理解工作原理的基础上找出下列说法不正确的是( )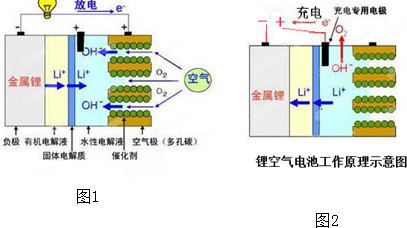

| A、锂空气电池配置了充电专用的阳极,可防止充电时空气极发生腐蚀和劣化.由于有固体电解质膜的存在,比普通锂电池更安全 |
| B、该电池放电时正极反应式为:O2+2H2O+4e-═4OH-.由于正极材料来源于空气,整个电池质量相同时,锂空气电池比普通锂电池能提供更多的电能 |
| C、锂空气电池电放完后也可以不必进行充电,只需要通过更换正极的水性电解液,并以合适的方式补给负极的金属锂,就可以连续使用 |
| D、在电池工作过程中,锂空气电池的空气极(多孔碳)附近电解液的pH逐渐降低 |
短周期元素X、Y、Z、W、Q在元素周期表中的位置如图所示,其中X元素的最外层电子数与其电子层数相同,则下列说法正确的是( )
| Y | Z | W | ||
| X | Q |
| A、元素Y、Z、W、Q均可与氢元素形成一种或多种氢化物,其中YH4中 H的质量分数最大 |
| B、由元素X与元素W组成的物质既能溶于足量的稀盐酸,又能溶于足量的氨水 |
| C、元素Y、Z、W的单质晶体一定是同种类型的晶体 |
| D、为了增强Q单质水溶液的漂白性,可将与W同主族且相邻的元素的低价氧化物通入其中 |
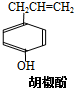 胡椒酚是植物挥发油中的一种成分.关于胡椒酚的下列说法,其中正确的是( )
胡椒酚是植物挥发油中的一种成分.关于胡椒酚的下列说法,其中正确的是( )①该化合物属于芳香烃;
②分子中至少有7个碳原子处于同一平面;
③它的部分同分异构体能发生银镜反应;
④1mol该化合物最多可与2mol Br2发生反应.
| A、①③ | B、①②④ |
| C、②③ | D、②③④ |
化学与社会、生活密切相关,下列有关说法不正确的是( )
| A、利用清洁能源代替化石燃料,有利于节约资源、保护环境 |
| B、食品添加剂苯甲酸钠,它是苯的一种同系物所对应的钠盐 |
| C、抗酸药的种类很多,如碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝、等 |
| D、乙醇属于可再生能源 |
将0.2mol/L的醋酸钠溶液与0.1mol/L盐酸等体积混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是( )
| A、c (Ac-)>c (Na+)>c (H+)>c (HAc) |
| B、c (Na+)+c (H+)=c (Ac-)+c (Cl-) |
| C、c (Ac-)=c (Cl-)>c (H+)>c (HAc) |
| D、c (Ac-)>c (Cl-)>c (HAc)>c(H+) |
 某班学生利用0.100mol?L-1的盐酸和0.100mol?L-1NaOH溶液反应测定酸碱滴定曲线.甲、乙、丙三组同学锥形瓶中的溶液所取体积均为20.00mL,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示:下列说法错误的是( )
某班学生利用0.100mol?L-1的盐酸和0.100mol?L-1NaOH溶液反应测定酸碱滴定曲线.甲、乙、丙三组同学锥形瓶中的溶液所取体积均为20.00mL,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示:下列说法错误的是( )| A、甲组同学滴定时选用的滴定管为酸式滴定管 |
| B、乙和丙两组同学的操作上都存在着失误 |
| C、乙组同学操作上的不足之处是在滴定终点附近测试和记录pH的间隔太大 |
| D、造成丙组同学的曲线与甲组同学不同的原因可能是用待装液润洗锥形瓶 |
短周期主族元素X、Y、Z、W的原子序数依次增大,X原子核外最外层电子数是次外层的2倍,Y的氟化物YF3分子中各原子均达到8电子稳定结构,Z是同周期中原子半径最大的元素,W的最高正价为+7价.下列说法正确的是( )
| A、XH4的沸点比YH3的高 |
| B、X与W形成的化合物和Z与W形成的化合物的化学键类型相同 |
| C、Y离子的半径比Z离子的半径小 |
| D、元素W的最高价氧化物对应水化物的酸性比Y的强 |