在恒温恒容密闭容器中进行合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92kJ?mol-1,下列选项中能表示该反应达到平衡状态的是 ( )(填字母序号).
| A、混合气体的压强不再发生变化 |
| B、混合气体的密度不再发生变化 |
| C、反应容器中N2、NH3的物质的量的比值不再发生变化 |
| D、单位时间内断开a个H-H键的同时形成3a个N-H键 |
| E、三种物质的浓度之比恰好等于化学方程式中各物质的化学计量数之比 |
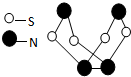 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图所示是已合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图所示是已合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )| A、该物质的分子式为SN |
| B、该物质与化合物S2N2互为同素异形体 |
| C、该物质在固态时形成原子晶体 |
| D、该物质的分子中既有极性键,又有非极性键 |
为监测空气中汞蒸气是否超标,通过悬挂涂有CuI(白色)的滤纸,根据滤纸是否变色(亮黄色至暗红色)及变色所需时间来判断空气中的汞含量.发生的化学反应为:4CuI+Hg=Cu2HgI4+2Cu.下列说法不正确的是( )
| A、上述反应属于置换反应 |
| B、该反应中的氧化剂与还原剂的物质的量之比为2:l |
| C、Cu2HgI4既是氧化产物又是还原产物 |
| D、当有1 mol CuI参与反应时,转移电子的物质的量为0.5 mol |
下列离子方程式中,不正确的是( )
| A、向NaHSO4溶液中加入过量的Ba(OH)2溶液:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| B、向Fe(OH)3中加入过量的HI溶液:Fe(OH)3+3H+=Fe3++3H2O |
| C、用淀粉碘化钾试纸和盐酸检验加碘盐:IO3-+5I-+6H+=3I2+3H2O |
| D、将少量SO2气体通入足量的NaClO溶液中:SO2+ClO-+H2O=SO42-+Cl-+2H+ |
下列说法正确的是( )
| A、用硝酸可鉴别由铜锌合金制成的假金币 |
| B、工业上常用电解熔融AlCl3,制备金属Al |
| C、Al(OH)3、Cu(OH)2均不能在氨水中溶解 |
| D、邻羟基苯甲酸的沸点比对羟基苯甲酸的高 |
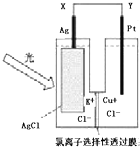 一种光化学电池的结构如图,当光照在表面涂有氯化银的银片上时,AgCl(s)═AgCl(s)=Ag (s)+Cl(AgCl),[Cl(AgCl)表示生成的氯原子吸附在氯化银表面],接着Cl(AgCl)+e--→Cl-(aq),若将光源移除,电池会立即回复至初始状态.下列说法正确的是( )
一种光化学电池的结构如图,当光照在表面涂有氯化银的银片上时,AgCl(s)═AgCl(s)=Ag (s)+Cl(AgCl),[Cl(AgCl)表示生成的氯原子吸附在氯化银表面],接着Cl(AgCl)+e--→Cl-(aq),若将光源移除,电池会立即回复至初始状态.下列说法正确的是( )| A、光照时,电流由Y流向X |
| B、光照时,Pt电极发生的反应为2Cl-+2e-═Cl2光 |
| C、光照时,Cl-向Ag电极移动 |
| D、光照时,电池总反应为:AgCl(s)+Cu+(aq)═Ag (s)+Cu2+(aq)+Cl-(aq) |
锂空气电池作为新一代大容量电池而备受瞩目,其工作原理如图所示.下列有关锂空气电池的说法不正确的是( )


| A、随着电极反应的不断进行,正极附近的电解液PH不断升高 |
| B、若把碱性电解液换成固体氧化物电解质,则正极会因为生成Li2O而引起碳孔堵塞,不利于正极空气的吸附 |
| C、放电时,当有22.4L O2(标准状况下)被还原时,溶液中有4mol Li+从左槽移动到右槽 |
| D、锂空气电池又称作“锂燃料电池”,其总反应方程为:4Li+O2═2Li2O |
某固体酸燃料电池以NaHSO4固体为电解质传递H+其基本结构见如图所示,电池总反应表示为:2H2+O2═2H2O下列有关说法正确的是( )


| A、电子通过外电路从b极流向a极 |
| B、H+由a极通过固体酸电解质传递到b极 |
| C、b极上的电极反应式为:O2+2H2O+4e-═4OH- |
| D、每转移0.1mol电子,消耗1.12L的H2 |
 短周期金属元素甲~戊在元素周期表中的相对位置如图所示.下列判断正确的是( )
短周期金属元素甲~戊在元素周期表中的相对位置如图所示.下列判断正确的是( )| A、原子半径:丙<丁<戊 |
| B、金属性:甲>丙 |
| C、氢氧化物碱性:丙>丁>戊 |
| D、最外层电子数:甲>乙 |
如图是回收利用H2S的工艺流程.下列说法不正确的是( )

| A、反应①的离子方程式:2Fe3++H2S═2Fe2++S↓+2H+ | ||||
| B、反应②中的阴极反应式为:2H++2e-═H2↑ | ||||
C、该流程的总反应式为:H2S
| ||||
| D、该过程中,能量转化形式有两种 |