下列表述中,合理的是( )
| A、用已知浓度的NaOH溶液测定盐酸的浓度,酸式滴定管未用待装溶液润洗会造成测定结果偏高 | ||||
B、Na2CO3溶液中:c(Na+)>c(CO
| ||||
| C、等体积等浓度的氢氧化钠与醋酸混合:c(Na+)=c(CH3COO-) | ||||
D、c(NH
|
下列反应属于取代反应的是( )
①CH3COOCH3+CH3CH2OH→CH3COOCH2CH3+CH3OH
②2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
③CH3CH2Br+NaOH→C2H4↑+NaBr+H2O
④C2H4+HCl→C2H5Cl.
①CH3COOCH3+CH3CH2OH→CH3COOCH2CH3+CH3OH
②2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
③CH3CH2Br+NaOH→C2H4↑+NaBr+H2O
④C2H4+HCl→C2H5Cl.
| A、①② | B、①④ | C、③④ | D、②③ |
镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在放电过程中的总反应方程式是:NiOOH+MH═Ni(OH)2+M,下列说法错误的是( )
| A、放电过程中负极的电极反应式:MH+OH--e-═H2O+M |
| B、放电过程中OH-从正极向负极迁移 |
| C、放电时若有1 mol M生成,则转移的电子数目为NA (NA为阿伏伽德罗常数的值) |
| D、NiMH电池中不能用KOH溶液作为电解质溶液 |
 将CH4和Cl2按体积比1:2混合充入大试管中,将此试管倒立在盛Na2SiO3溶液的水槽里,放在光亮处,如图所示下列描述正确的是( )
将CH4和Cl2按体积比1:2混合充入大试管中,将此试管倒立在盛Na2SiO3溶液的水槽里,放在光亮处,如图所示下列描述正确的是( )| A、由于Cl2不足,生物中不含有CHCl3、CCl4 |
| B、CH4和Cl2取代的产物全部都是极性分子 |
| C、水槽底部出现白色沉淀 |
| D、最终试管内全部充满溶液 |
一定量的稀硫酸跟过量铁粉反应,为了减缓反应速率,又不影响生产氢气的总量,可向稀硫酸中加入适量的( )
| A、Ca(OH)2固体 |
| B、NH4Cl(固体) |
| C、CuSO4(溶液) |
| D、CH3COONa(固体) |
下列物质中,均直接由原子构成的是( )
①干冰晶体;②二氧化硅;③水蒸气;④金刚石;⑤单晶硅;⑥白磷;⑦硫磺;⑧液氨;⑨钠和氖晶体.
①干冰晶体;②二氧化硅;③水蒸气;④金刚石;⑤单晶硅;⑥白磷;⑦硫磺;⑧液氨;⑨钠和氖晶体.
| A、②④⑤ | B、②③④⑤⑨ |
| C、②③④⑤ | D、②④⑤⑥⑦⑨ |
下面有关氯化铯晶体的叙述中,不正确的是( )
| A、1mol氯化铯中有N 个CsCl分子 |
| B、氯化铯晶体中,每个Cs+周围距离相等的Cs+共有6个 |
| C、氯化铯晶体中,每个Cs+周围紧邻8个C1- |
| D、平均每个Csc1晶胞中有1个Cs+、1个C1- |
| E、平均每个Csc1晶胞中有1个Cs+、1个C1- |
设NA为阿伏伽德罗常数.下列叙述正确的是( )
| A、1mol甲醇中含有C-H键的数目为4NA |
| B、标准状况下,2.24L已烷含有分子的数目为0.1NA |
| C、12克金刚石中含有的共价键数目为2NA |
| D、1 mol 甲基所含的电子数为10NA |
已知某反应aA(g)+bB(g)?═?cC(g)的各物质浓度数据如下:据此可推算出a:b:c是( )
| A | B | C | |
| 起始浓度(mol?L-1) | 3.0 | 1.0 | 0 |
| 2s末浓度(mol?L-1) | 1.8 | 0.6 | 0.8 |
| A、9:3:4 |
| B、3:1:2 |
| C、2:1:3 |
| D、3:2:1 |
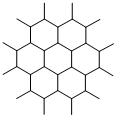 2010年诺贝尔物理学奖用于表彰首次剥离出单层石墨的科学家.单层石墨称为石墨烯,这种“只有一层碳原子厚的碳薄片”的石墨烯,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料.下列叙述正确是( )
2010年诺贝尔物理学奖用于表彰首次剥离出单层石墨的科学家.单层石墨称为石墨烯,这种“只有一层碳原子厚的碳薄片”的石墨烯,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料.下列叙述正确是( )| A、石墨烯和金刚石互为同分异构体 |
| B、石墨烯是一种有机物 |
| C、石墨烯中碳原子与共价键的个数比为1:3 |
| D、石墨烯可导电,但它不是电解质 |