下列化学(或离子)方程式正确的是( )
| A、乙酸与碳酸钠溶液反应:2H++CO32-═CO2↑+H2O | |||
B、C6H6+HNO3
| |||
| C、亚硫酸的电离方程式:H2SO3?2H++SO32- | |||
| D、醋酸溶液与新制氢氧化铜反应:CH3COOH+OH-→CH3COO-+H2O |
下列化合物,按其晶体的熔点由低到高排列正确的是( )
| A、SiO2 CsCl I2 Br2 |
| B、SiO2 CsCl Br2 I2 |
| C、CsCl SiO2 I2 Br2 |
| D、Br2 I2 CsCl SiO2 |
能使紫色石蕊试液变色的物质是( )
| A、乙酸 | B、甲烷 | C、乙醇 | D、苯 |
乙醇分子中不同的化学键如图所示,关于乙醇有关性质的说法不正确的是( )
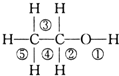

| A、和金属钠反应键①断裂 |
| B、在铜催化下和O2反应键①④断裂 |
| C、乙醇与金属钠反应比水与金属钠反应缓慢 |
| D、钠与乙醇反应时,钠熔化成一个小球在乙醇表面不断的游动 |
“绿色化学”又称环境无害化学、环境友好化学、清洁化学,某化学课外小组利用废铜制取硫酸铜,设计了如下制取方案,其中符合“绿色化学”要求的是( )
A、Cu
| ||||||
B、Cu
| ||||||
C、Cu
| ||||||
D、Cu
|
如图中a、b、c、d、e、f为元素周期表中前4周期的一部分元素,下列有关叙述正确的是( )
| a | ||||
| b | c | |||
| d | e | |||
| f |
| A、b、c、e三种元素的原子半径大小关系:e>c>b |
| B、六种元素分别形成的单质固体中,d的熔、沸点最高 |
| C、c的氢化物沸点比f的氢化物沸点低 |
| D、b元素除0价外,只有一种化合价 |
下列说法正确的是( )
A、已知0.1 mol?L-1的醋酸溶液中存在电离平衡:CH3COOH?CH3COO-+H+,加少量烧碱溶液可使溶液中
| ||
| B、饱和纯碱 (Na2CO3)溶液中:2c(Na+)═c(CO32-)+c(HCO3-)+c(H2CO3) | ||
| C、将0.2mol/L的某一元弱酸HA溶液和0.1mol/L NaOH溶液等体积混合,则充分反应后的混合液中:2c(OH-)+c(A-)═2c(H+)+c(HA) | ||
| D、pH相等的CH3COONa溶液、C6H5ONa溶液和NaOH溶液,其物质的量浓度由小到大的顺序为:c(NaOH)<c(CH3COONa)<c(C6H5ONa) |
下列说法正确的是( )
| A、原子的电子层数越多,原子半径越大 |
| B、同族元素相差的原子序数可能为16、26、36、46 |
| C、ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
| D、卤族元素的单质均有氧化性,最高正价都是+7 |
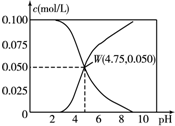 25℃时,有c(CH3COOH)+c(CH3COO-)=0.1mol?L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-) 与pH的关系如图所示.下列有关溶液中离子浓度关系的叙述中不正确的是( )
25℃时,有c(CH3COOH)+c(CH3COO-)=0.1mol?L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-) 与pH的关系如图所示.下列有关溶液中离子浓度关系的叙述中不正确的是( )| A、pH=5.5的溶液中c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) |
| B、W点所表示的溶液中c(Na+)+c(H+)═c(CH3COOH)+c(OH-) |
| C、pH=3.5的溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)═0.1mol?L-1 |
| D、向W点所表示的1L溶液中通入0.05mol HCl气体(溶液的体积变化可忽略):c(H+)═c(OH-)+c(CH3COOH) |
某恒温密闭容器中,可逆反应A(s)?B+C(g)△H=+Q kJ?mol-1(Q>0)达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )
| A、产物B的状态只能为固态或液态 |
| B、平衡时,单位时间内n(A)消耗﹕n(C)消耗=1﹕1 |
| C、若开始时向容器中加入1molB和1molC,达到平衡时放出热量QkJ |
| D、保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动 |