下列说法中,正确的是( )
A、 -OH与 -OH与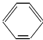 -CH2OH互为同系物 -CH2OH互为同系物 |
| B、乙醇和乙醚互为同分异构体 |
| C、乙醇、乙二醇、丙三醇互为同系物 |
| D、可用浓溴水来区分乙醇苯酚 |
核电荷数小于18的某元素X,某原子核外电子层数为a,最外层电子数为(2a+1),下列有关元素X的说法中,不正确的是( )
| A、元素X的原子核内质子数为(2a2-1) |
| B、元素X的原子半径一定小于钠的原子半径 |
| C、由元素X形成的某些化合物,可能具有杀菌消毒的作用 |
| D、元素X形成的简单离子,各电子层的电子数均达到2n2个(n表示电子层数) |
在室温下等体积的酸和碱的溶液,混合后pH一定小于7的是( )
| A、pH=2的硝酸和pH=12的Ba(OH)2溶液 |
| B、pH=3的盐酸和pH=11的氨水 |
| C、pH=3的硫酸和pH=11的KOH |
| D、pH=4的醋酸和pH=10的KOH溶液 |
下列关于胶体的叙述中,正确的是( )
| A、胶体是一种分散质直径小于10-10m的分散系 |
| B、胶体一定是液态的 |
| C、用一束光线照射胶体,在垂直于光线的方向可看到一条光亮的通路 |
| D、蛋白质溶液不是一种胶体 |
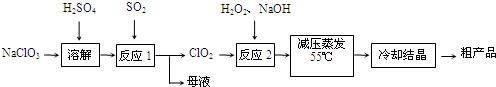

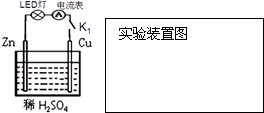 (1)原电池是一种将
(1)原电池是一种将