已知A、B、C、D是短周期中原子序数依次增大的4种主族元素,其中元素A、C为处于同主族的非金属元素,其单质在常温下都呈固态.元素B的原子最外层电子数与电子层数相等,元素D在同周期元素中非金属性最强.下列说法正确的是( )
| A、原子半径:A<B<C<D |
| B、气态氢化物的稳定性:D>C |
| C、最高价氧化物对应水化物的酸性:A<C |
| D、常温下单质B能溶于浓硫酸 |
某课外研究小组的同学将FeCl3(aq)滴加到5%H2O2溶液后,发现产生无色气体由慢到快,最后再变慢;溶液温度升高;同时溶液颜色由黄色立即变为棕褐色,当反应殆尽时,溶液又恢复黄色,由此得出以下结论,你认为错误的是( )
| A、H2O2的分解反应为放热反应 |
| B、FeCl3是H2O2分解反应的催化剂 |
| C、与不加FeCl3(aq)相比,当H2O2均完全分解时,加FeCl3(aq)使反应放出的热量更多 |
| D、若将少量FeCl2溶液滴入过量5%H2O2溶液中,则除溶液颜色变化不同外,其它现象相同 |
下列各组物质中,关系不正确的是( )
| A、H2和T2 互为同素异形体 | ||||
B、
| ||||
| C、乙醇和二甲醚互为同分异构体 | ||||
| D、苯和甲苯互为同系物 |
下列有关说法正确的是( )
| A、2H2(g)+O2(g)=2H2O(g)△H=-483.6KJ?mol-1,则氢气的燃烧是241.8KJ?mol-1 | ||||||
| B、对于密闭容器中反应3H2(g)+N2(g)?2NH3(g)△H=-92.4kJ?mol-1,3molH2与1molN2完全反应放出92.4kJ热量. | ||||||
| C、各种平衡常数,无论k、Ka、Kb、KW、KSP都随温度的改变而改变 | ||||||
D、反应2HI(g)?H2(g)+I2 (g) 在448℃时,其平衡常数为
|
25℃时PH=7的(NH4)2SO4与NH3?H2O混合溶液中
的值为( )
| c(NH4+) |
| c(SO42-) |
| A、大于2 | B、等于2 |
| C、小于2 | D、无法确定 |
已知,下列反应可以发生:Br2+H2SO3+H2O=2HBr+H2SO4,在100mL含等物质的量HBr和H2SO3的溶液里通入0.01molCl2,有一半Br-变为Br2.原溶液中HBr和H2SO3的浓度都等于( )
| A、0.0075mol/L |
| B、0.0018mol/L |
| C、0.075mol/L |
| D、0.08mol/L |
室温下,某溶液中由水电离出的H+和OH-物质的量浓度乘积为1×10-28,该溶液中一定不能大量共存的是( )
| A、Cl-、AlO2-、K+、Na+ |
| B、Fe2+、NO3-、Ba2+、Cl- |
| C、Fe3+、SO42-、MnO4-、Na+ |
| D、Na+、K+、CO32-、SO42- |
对于化学反应:2Na+2H2O═2NaOH+H2↑的有关叙述错误的是( )
| A、该反应中既有旧化学键的断裂,也有新化学键的生成 |
| B、该反应中每消耗1molNa,则同时消耗18gH2O,产生1molNaOH和11.2LH2(标况下) |
| C、由于该反应常温下能自动进行,所以该反应一定是放热反应 |
| D、由于该反应是放热反应,所以断裂旧化学键所吸收的能量一定比形成新化学键所放出的能量少 |
为维持生命活动,人需要不断地补充能量.下列物质中不能为人补充能量的是( )
| A、水 | B、糖类 | C、油脂 | D、蛋白质 |
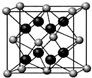 萤石(CaF2)晶体属于立方晶系如图所示,萤石中每个Ca2+被8个F-所包围,则每个F-周围最近距离的Ca2+数目为( )
萤石(CaF2)晶体属于立方晶系如图所示,萤石中每个Ca2+被8个F-所包围,则每个F-周围最近距离的Ca2+数目为( )