0 133669 133677 133683 133687 133693 133695 133699 133705 133707 133713 133719 133723 133725 133729 133735 133737 133743 133747 133749 133753 133755 133759 133761 133763 133764 133765 133767 133768 133769 133771 133773 133777 133779 133783 133785 133789 133795 133797 133803 133807 133809 133813 133819 133825 133827 133833 133837 133839 133845 133849 133855 133863 203614

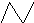 ,有机物A的键线式结构为
,有机物A的键线式结构为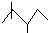 ,有机物B与等物质的量的H2发生加成反应可得到有机物A.则:
,有机物B与等物质的量的H2发生加成反应可得到有机物A.则: