下列说法不正确的是( )
| A、NaClO、NaClO2、KClO3、NaClO4中Cl的化合价依次升高 |
| B、C与CuO高温共热,C的氧化产物只能是CO2 |
| C、H2SO4由分子构成,溶于水离解成H+和SO42- |
| D、Al与Fe2O3高温反应生成Al2O3与Fe,属于置换反应 |
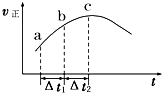 向绝热恒容密闭容器中通入SO2和NO2,一定条件下使可逆反应SO2(g)+NO2(g)?SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示.由图可得出正确的结论是( )
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使可逆反应SO2(g)+NO2(g)?SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示.由图可得出正确的结论是( )| A、反应在 c 点达到平衡状态 |
| B、反应物浓度:a 点小于 b 点 |
| C、反应物的总能量低于生成物的总能量 |
| D、△t1=△t2 时,SO2 的转化率:a~b 段小于 b~c 段 |
氢化钠(NaH)化合物中钠元素是+1价,NaH跟水反应放出H2,下列叙述正确的是( )
| A、在NaH中的氢离子半径比锂离子半径大 |
| B、在NaH中的氢离子的电子层排布与氦原子不相同 |
| C、NaH跟水反应后溶液呈酸性 |
| D、NaH中的氢离子被还原成氢气 |
一定温度下,将1mollCO与2molH2和催化剂一起放入容积恒定密闭容器中反应:CO(g)+2H2(g)?CH3OH.测得平衡时生成CH3OH0.65mol.若此时再通入H2 2mol.则重新达到平衡时,CH3OH的物质的量可能是( )
| A、0.65 | B、0.72 |
| C、1.00 | D、1.30 |
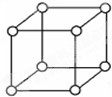 查资料表知,只有钋的晶体中的原子具有如图所示的堆积方式,钋的外围电子排布式是6s26p4.下列关于钋的说法错误的是( )
查资料表知,只有钋的晶体中的原子具有如图所示的堆积方式,钋的外围电子排布式是6s26p4.下列关于钋的说法错误的是( )| A、右图的堆积方式空间利用率太低,金属极少采取这种堆积方式 |
| B、钋晶体中原子的配位数为 6 |
| C、钋基态原子的能层数=周期序数=价电子数 |
| D、钋的常见化合价为+4、+6、-2价 |
下列说法正确的是( )
| A、丙烷是直链烃,所以分子中3个碳原子也在一条直线上 |
| B、丙烯所有原子均在同一平面上 |
C、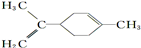 所有碳原子一定在同一平面上 所有碳原子一定在同一平面上 |
D、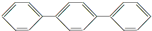 至少有16个原子共平面 至少有16个原子共平面 |
实验室用NaCl固体配400mL 1.0mol/L NaCl溶液,下列判断不对的是( )
| A、用托盘天平称取NaCl固体23.4g |
| B、应选用500mL的容量瓶来配制此溶液 |
| C、在转移操作中不慎将溶液洒到容量瓶外面,应该重新配置溶液 |
| D、加蒸馏水至离刻度线1-2cm时改用胶头滴管定容 |
下列物质所含的原子与0.1mol H3PO4所含的原子数目相等的是( )
| A、0.2mol H2O2 |
| B、0.1mol H2SO4 |
| C、0.2mol NaOH |
| D、0.3mol H2O |
某澄清透明溶液中可能含有:NH4+、Ba2+、Al3+、Fe2+、SO32-、SO42-、HCO3-中的几种离子.为确定溶液组成,进行如下实验:
①测定溶液的pH,溶液显强酸性.滴加Ba(NO3)2(aq)出现白色沉淀.
②取少量溶液加入NaOH(aq)至强碱性,产生刺激性气味的气体并得到澄清溶液.
③在②的澄清溶液中通入足量CO2,有白色沉淀生成.
由此,正确的推测是( )
①测定溶液的pH,溶液显强酸性.滴加Ba(NO3)2(aq)出现白色沉淀.
②取少量溶液加入NaOH(aq)至强碱性,产生刺激性气味的气体并得到澄清溶液.
③在②的澄清溶液中通入足量CO2,有白色沉淀生成.
由此,正确的推测是( )
| A、一定有Al3+离子 |
| B、可能有HCO3-离子 |
| C、不能确定SO32-离子是否存在 |
| D、不存在Fe2+离子,可能存在Ba2+离子 |