两种气态烃以任意比例混合,在105℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得到气体体积是11L.下列各组混合烃符合此条件的是( )
| A、C4H10、C3H6 |
| B、C4H8、C3H8 |
| C、C4H10、C2H4 |
| D、CH4、C3H8 |
单质碘的熔沸点较低,其原因是( )
| A、碘的非金属性较弱 |
| B、碘分子中键能较小 |
| C、碘晶体中碘分子间以范德华力结合 |
| D、I-I共价键的键长较长 |
共价键、离子键和范德华力都是微粒之间的作用力,下列含有上述两种结合力的是( )
①Na2O2 ②SiO2 ③干冰 ④金刚石 ⑤NaCl ⑥白磷.
①Na2O2 ②SiO2 ③干冰 ④金刚石 ⑤NaCl ⑥白磷.
| A、①②④ | B、①③⑥ |
| C、②④⑥ | D、③④⑤ |
用铁片与稀硫酸反应时,下列措施不能使反应速率加快的是( )
| A、加热 |
| B、不用稀硫酸,改用98%浓硫酸 |
| C、滴加少量的ZnSO4溶液 |
| D、不用铁片,改用铁粉 |
关于如图所示装置的叙述中正确的是( )
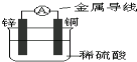

| A、当有0.2mol电子通过电路,产生H2体积为2.24L |
| B、电子从锌片经金属导线流向铜片 |
| C、铜片质量逐渐减少 |
| D、溶液中的氢离子向锌电极移动 |
下列装置或操作能达到实验目的是( )
A、 除去乙醇中的乙酸 |
B、 形成原电池 |
C、 铝热反应 |
D、 石油的蒸馏 |
下列的晶体中,化学键种类相同、晶体类型也相同的是( )
| A、SO3与SiO2 |
| B、NO2与H2O |
| C、NaCl与HCl |
| D、CCl4与KCl |
下列各组离子在对应溶液中可能大量存在的是( )
| A、水电离出的c(H+)=10-12 mol?L-1的溶液:K+、Cu2+、SO32-、MnO4- |
| B、与铝粉反应能放出氢气的溶液:Na+、SO42-、HCO3-、Cl- |
| C、含有大量ClO-的溶液:H+、I-、SO42-、Cl- |
| D、pH=12的溶液:K+、Cl-、SO32-、SiO32- |
下列实验方案不合理的是( )
| A、鉴别集气瓶中的甲烷和乙烯:移去玻璃片,分别点燃,观察火焰颜色及是否有黑烟 |
| B、制备氯乙烷(C2H5Cl):将乙烷和氯气的混合气体放在光照条件下反应 |
| C、从碘水中提取单质碘时,可用苯代替CCl4 |
| D、向氨水中滴加Al2(SO4)3溶液和向Al2(SO4)3溶液滴加氨水现象相同 |
合成氨的热化学方程式为N2(g)+3H2(g)2NH3(g)△H=-92.4kJ?mol-1.现将1molN2(g)、3molH2(g)充入一容积为2L的密闭容器中,在500℃下进行反应,10min时达到平衡,NH3的体积分为?,下列说法中正确的是
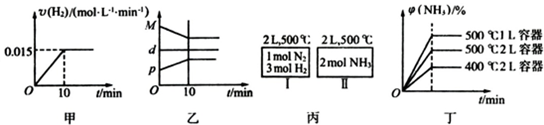 ( )
( )
 ( )
( )| A、若达到平衡时,测得体系放出9.24kJ热量,则H2反应速率变化曲线如图甲所示 |
| B、反应过程中,混合气体平均相对分子质量为M,混合气体密度为d,混合气体压强为p,三者关系如图乙 |
| C、如图丙所示,容器I和II达到平衡时所需要的时间可能不同 |
| D、若起始加入物料为1 mol N2,3 mol H2,在不同条件下达到平衡时,NH3的体积分数变化如图丁所示 |