下列反应的离子方程式书写正确的是( )
| A、电解饱和食盐水:2Cl-+2H+=H2↑+Cl2↑ |
| B、浓盐酸与二氧化锰反应制氯气:MnO2+2Cl-+2H+=Cl2↑+Mn2++H2O |
| C、用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| D、向溴化亚铁溶液中通入过量的氯气:2Fe2++Cl2=2Cl-+2Fe3+ |
MgCl2溶液中能够大量共存的一组离子是( )
| A、H+、NH4+、Na+、NO3- |
| B、OH-、NO3-、K+、CO32- |
| C、HCO 3 -、H+、Na+、SO42- |
| D、H+、Ag+、NO3-、Ca2+ |
下列表示对应化学反应的离子方程式正确的是( )
A、向氯化铝溶液通入过量的氨气:Al3++4OH-═
| ||||
B、MnO2与浓盐酸反应制Cl2:MnO2+4HCl
| ||||
| C、FeCl3溶液用于蚀刻印刷电路:Cu+2Fe3+=Cu2++2Fe2+ | ||||
| D、在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+Fe(OH)3=FeO42-+3Cl-+H2O+4H+ |
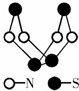 如图是已经合成的最著名硫-氮化合物分子结构.下列说法正确是( )
如图是已经合成的最著名硫-氮化合物分子结构.下列说法正确是( )| A、该物质的分子式为SN |
| B、该物质中的N原子最外层都达到8电子稳定结构 |
| C、该物质的分子中既有极性键又有非极性键 |
| D、该物质与化合物S2N2互为同素异形体 |
已知:C(s)+O2(g)=CO2(g);△H=-393.5kJ/mol
H2(g)+
O2(g)=H2O(l);△H=-241.8kJ/mol
欲得到相同的热量,需分别燃烧固体碳和氢气的质量比约为( )
H2(g)+
| 1 |
| 2 |
欲得到相同的热量,需分别燃烧固体碳和氢气的质量比约为( )
| A、2:3.25 |
| B、12:3.25 |
| C、1:1 |
| D、393.5:241 |
下列关于自发反应的说法中正确的是( )
| A、在一定条件下,自发反应的逆过程一定是非自发的 |
| B、自发反应一定能进行,非自发反应一定不能进行 |
| C、自发反应一定能进行彻底 |
| D、可以通过改变温度或加催化剂的办法使非自发反应转变为自发反应 |
下列烯烃和HBr发生加成反应,所得的产物有同分异构体的是( )
| A、CH2=CH2 |
| B、CH3CH=CHCH3 |
| C、CH3CH=CH2 |
| D、CH3CH2CH=CHCH2CH3 |
有甲、乙两位同学分别做碳酸钠溶液和盐酸反应的实验.甲同学将80ml 1mol?L-1的碳酸钠溶液逐滴加入到100ml 1mol?L-1的盐酸中去;乙同学则将100ml 1mol?L-1的盐酸逐滴加入到80ml 1mol?L-1的碳酸钠溶液中去,甲、乙两位同学产生的CO2气体的体积比为( )
| A、1:1 | B、4:5 |
| C、5:2 | D、5:4 |
下列分子或离子的中心原子没有采取sp3杂化的是( )
| A、晶体硅中的硅原子 |
| B、NH4+ |
| C、BF3 |
| D、ClO4- |
用酸性氢氧燃料电池电解苦卤水 (含Cl-、Br-、Na+、Mg2+)的装置如图所示 (a、b为石墨电极).下列说法中,正确的是( )
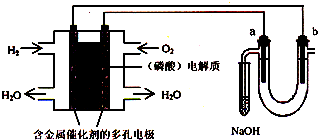

| A、电池工作时,正极反应式为:O2+2 H2O+4e-=4OH- |
| B、忽略能量损耗,当电池中消耗0.02g H2时,a极周围会产生0.02g H2 |
| C、电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极 |
| D、电解时,a 电极周围首先放电的是Br-而不是Cl-,说明当其它条件相同时Br-的还原性强于Cl- |