0 133513 133521 133527 133531 133537 133539 133543 133549 133551 133557 133563 133567 133569 133573 133579 133581 133587 133591 133593 133597 133599 133603 133605 133607 133608 133609 133611 133612 133613 133615 133617 133621 133623 133627 133629 133633 133639 133641 133647 133651 133653 133657 133663 133669 133671 133677 133681 133683 133689 133693 133699 133707 203614
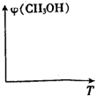 工业上在合成塔中采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=QkJ/mol
工业上在合成塔中采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=QkJ/mol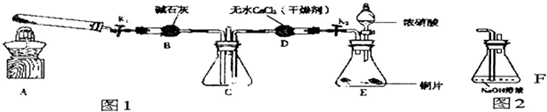
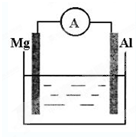 如图所示,组成一个原电池.
如图所示,组成一个原电池.