经研究发现,有一种磷分子具有链状结构,其结构简式为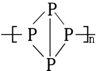 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A、它是一种高分子化合物 |
| B、它的分子中具有极性共价键 |
| C、分子中每个磷原子以三个共价健分别结合三个磷原子 |
| D、分子中具有不饱和键 |
混合气体由O2和CH4组成,测得混合气体在标准状况下的密度为0.892g/L,则混合气体中O2和CH4的体积之比为( )
| A、1:1 | B、1:3 |
| C、4:1 | D、1:2 |
某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO3-的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为( )
| A、21:5 | B、11:3 |
| C、3:1 | D、4:1 |
酒精燃烧的化学方程式为:C2H6O+3O2═2CO2+3H2O,完全燃烧一定量的无水酒精,放出的热量为Q,当完全吸收生成的CO2,消耗8mol/L的NaOH溶液50ml时恰好生成正盐.则燃烧1mol无水酒精所放出的热量为( )
| A、0.2Q | B、0.1Q |
| C、5Q | D、10Q |
100ml 6mol?L-1H2SO4与过量的锌粉反应,在一定温度下,为了减缓反应速率,又不影响生成H2的总量,可向反应混合物中加入适量的( )
| A、K2SO4溶液 |
| B、KNO3溶液 |
| C、醋酸 |
| D、NaHSO4固体 |
下列说法或做法正确的是( )
| A、黑色金属材料通常包括铁、铬、锰以及它们的合金 |
| B、镁在空气中燃烧的产物只有MgO |
| C、海水提镁和海水提溴所涉及的化学反应全都是氧化还原反应 |
| D、用量筒量取10.0mL1.0mol?L-1 的盐酸于100mL容量瓶中,加水稀释至刻度,可制得0.1mol?L-1 的盐酸 |
阿伏伽德罗常数约为6.02×1023mol-1,下列叙述正确的是( )
| A、1mol H2O2中含NA个H2和NA个O2 |
| B、氧气和臭氧的混合物16g中约含有6.02×1023个氧原子 |
| C、25℃时,含40g氢氧化钠的溶液中约含有6.02×1022个氢氧根离子 |
| D、0.5mol CH4中约含有3.01×1024个电子 |
下列各组物质的熔点变化规律,与它们的化学键无关的是( )
| A、F2、Cl2、Br2、I2的熔点依次升高 |
| B、Li、Na、K、Rb的熔点依次降低 |
| C、NaF、NaCl、NaBr、NaI的熔点依次降低 |
| D、晶体硅、碳化硅、金刚石熔点依次升高 |
下列物质必须隔绝空气和水蒸气保存的是( )
①Na ②NaOH ③Na2O ④Na2O2 ⑤Na2CO3 ⑥NaClO.
①Na ②NaOH ③Na2O ④Na2O2 ⑤Na2CO3 ⑥NaClO.
| A、①④ | B、②③④⑤ |
| C、①②③④ | D、①②③④⑥ |
下列热化学方程式或离子方程式中,正确的是( )
| A、甲烷的燃烧热为890.3 kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ?mol-1 | ||||||||
| B、500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中完全反应生成NH3(g),放热19.3 kJ,其热化学方程式为: N2(g)+3H2(g)
| ||||||||
| C、氯化镁溶液与氨水反应:Mg 2++2OH -=Mg(OH)2↓ | ||||||||
D、已知强酸与强碱的稀溶液反应的中和热为57.3 KJ/mol,则0.1mol醋酸与0.1mol氢氧化钠的稀溶液反应的热化学方程式为:
|