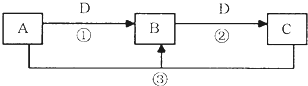
0 133467 133475 133481 133485 133491 133493 133497 133503 133505 133511 133517 133521 133523 133527 133533 133535 133541 133545 133547 133551 133553 133557 133559 133561 133562 133563 133565 133566 133567 133569 133571 133575 133577 133581 133583 133587 133593 133595 133601 133605 133607 133611 133617 133623 133625 133631 133635 133637 133643 133647 133653 133661 203614
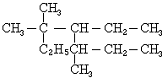 A.某烃与2倍的氢气加成后得到2,2-二甲基丁烷,按系统命名法,该烃的名称
A.某烃与2倍的氢气加成后得到2,2-二甲基丁烷,按系统命名法,该烃的名称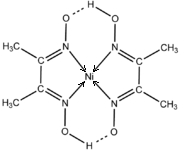 决定物质性质的重要因素是物质结构.请回答下列问题.
决定物质性质的重要因素是物质结构.请回答下列问题. 以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一.
以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一.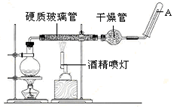 常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.
常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.