有关氨的性质的叙述中正确的是( )
| A、氨不能在空气中燃烧 |
| B、氨水呈碱性 |
| C、氨气和酸相遇能产生白色烟雾 |
| D、在反应 NH3+H+=NH4+ 中,氨失去电子被氧化 |
下列各种实验中不能达到实验目的是( )
A、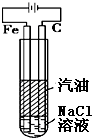 制备Fe(OH)2白色沉淀 |
B、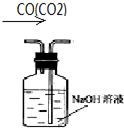 除去CO气体中的CO2气体 |
C、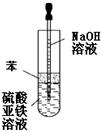 制备Fe(OH)2白色沉淀 |
D、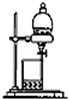 分离互不相溶的两种液体 |
叠氮酸(HN3)与醋酸酸性相似,下列叙述中一定错误的是( )
| A、HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(N3-)>c(OH-) |
| B、HN3与NH3作用生成的叠氮酸铵是共价化合物 |
| C、NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3-)>c(OH-)>c(H+) |
| D、N3-与CO2含相等电子数 |
下列实验操作中正确的是( )
| A、用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
| B、蒸馏操作时,应使温度计水银球插入蒸馏烧瓶中液体的液面下,但不能接触瓶底 |
| C、用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干 |
| D、萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
常温下,柠檬水溶液的PH是3,其中的C(OH-)是( )
| A、0.1mol/L |
| B、1.0×10-3 mol/L |
| C、1.0×10-11mol/L |
| D、1.0×10-7mol/L |
下列实验操作或对实验现象的解释错误的是( )
| A、由于氨极易溶于水,盛有10mL氨气的试管倒立在7mL水中,溶液不会充满试管 |
| B、为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化 |
| C、用酒精灯加热铝箔至熔化,铝并不滴落,说明铝表面生成了一层致密的氧化膜 |
| D、某试液中加入盐酸酸化的硝酸钡溶液,即使出现白色沉淀,也不能判断原试液中一定含有SO42- |
在盐酸滴定NaOH溶液的实验中,以酚酞试液作指示剂,滴定到终点时颜色变化是( )
| A、由无色变红色 |
| B、由红色变无色 |
| C、由红色变蓝色 |
| D、由蓝色变红色 |
实验中需1mol/L的NaOH溶液950mL,配制时应选用的容量瓶的规格和称取NaOH的质量分别是( )
| A、1000mL,40g |
| B、950mL,43.4g |
| C、任意规格,57.2g |
| D、500mL,28.6g |
某同学欲配制符合下列条件的溶液,其中可能实现的是( )
A、只含0.1 mol Na+、0.2 mol Mg2+、0.1 mol Cl-和0.1 mol NO
| ||||
B、只含0.1 mol NH
| ||||
| C、为了通过测定pH的大小,达到比较HCl和CH3COOH酸性强弱的目的,分别配制100 mL 0.1mol/L的NaCl溶液和CH3COONa溶液 | ||||
| D、仅用1 000 mL的容量瓶、烧杯、玻璃棒、量筒、58.5 g NaCl固体和水配制1 L 1 mol/L的NaCl溶液 |
下列化学用语正确的是( )
| A、Fe2(SO4)3与氨水反应:Fe3++3OH-=Fe(OH)3↓ |
| B、NaHCO3溶解于水电离:NaHCO3?Na++H++CO32- |
| C、NaHS的水解:HS-+H2O?H2S+OH- |
| D、Na2SO3的水解:SO32-+2H2O?H2SO3+2OH- |