配制250mL 0.10mol/L的NaOH溶液时,下列实验操作会使配得的溶液中NaOH物质的量浓度偏大的是( )
| A、转移溶液后未洗涤烧杯和玻璃棒就直接定容 |
| B、溶解后立即转移至容量瓶 |
| C、在容量瓶中定容时俯视刻度线 |
| D、定容后把容量瓶倒置摇匀,发现液面低于刻度线,又补足了所缺的水 |
NA为阿伏加德罗常数,下列叙述正确的是( )
A、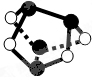 0.5mol雄黄(As4S4,已知As和N同主族,结构如图)含有NA个S-S键 |
| B、用惰性电极电解1 L浓度均为2 mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 NA个电子转移时,阴极析出6.4g金属 |
| C、1mol过氧化氢分子中共用电子对数为3NA |
| D、0.1mol Na2CO3?10H2O在晶体中或溶液中,含有的CO32-离子均小于0.1 NA |
分类是学习和研究化学的一种常用的科学方法.下列有关分类合理的有( )
①根据酸分子所含的氢原子数目的多少将酸分为一元酸、二元酸等
②根据反应中电子是否转移可将化学反应分为氧化还原反应和非氧化还原反应
③根据是否会产生丁达尔效应,可将分散系分为溶液、胶体、浊液
④根据物质的导电性可将物质分为导体、半导体和绝缘体.
①根据酸分子所含的氢原子数目的多少将酸分为一元酸、二元酸等
②根据反应中电子是否转移可将化学反应分为氧化还原反应和非氧化还原反应
③根据是否会产生丁达尔效应,可将分散系分为溶液、胶体、浊液
④根据物质的导电性可将物质分为导体、半导体和绝缘体.
| A、②③ | B、②④ | C、③④ | D、①②④ |
不能由单质直接化合而得到的化合物是( )
| A、FeCl3 |
| B、SO2 |
| C、NO2 |
| D、FeS |
配制0.1mol/LCuSO4溶液,可采用的方法是( )
| A、将25g胆矾溶于1L水中 |
| B、将25g胆矾溶于水,配成1L溶液 |
| C、取16g胆矾溶于水,再稀释到1L |
| D、称取16g无水CuSO4,溶于水配成1L溶液 |
醋酸溶液中存在电离平衡:CH3COOH?CH3COO-+H+,下列叙述中不正确的是( )
| A、升高温度时H+浓度增大 |
| B、加水稀释时平衡向右移动 |
| C、加入少量NaOH时溶液pH减小 |
| D、溶液中水电离出的H+浓度等于OH-浓度 |
中学化学中有许多规律,下列说法正确的是( )
| A、由卤族元素性质变化规律,类推同主族元素自上而下单质熔沸点一定是由低到高 |
| B、利用复分解反应以强制弱规律,弱酸一定不能制强酸 |
| C、能和碱反应生成盐和水的氧化物一定是非金属氧化物 |
| D、有单质参加和生成的反应不一定是氧化还原反应 |
1mol 某烃在O2中充分燃烧,需要消耗O2 179.2L(标准状况下).它在光照的条件下与Cl2反应能生成三种不同的一氯取代物.该烃的结构简式是( )
| A、CH3C(CH3)2CH2CH3 |
| B、CH3CH2CH2CH2CH3 |
| C、CH3CH2CHCH3 |
D、 |
下列各组离子中,在给定条件下能大量共存的是( )
| A、在pH=1的溶液中:NH4+、K+、ClO-、Cl- |
| B、有SO42-存在的溶液中:Na+、Mg2+、Ca2+、I- |
| C、有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- |
| D、在c(H+)=1.0×10-13mol?L-1的溶液中:Na+、S2-、[Al(OH)4]-、SO32- |
下列说法不正确的是( )
| A、所有的复分解反应都是非氧化还原反应 |
| B、液氨、液氯、液态氯化氢都是非电解质 |
| C、静电除尘利用了胶体能发生电泳的性质 |
| D、使空气中游离态的氮转化为含氮化合物的方法叫做氮的固定 |