0 133431 133439 133445 133449 133455 133457 133461 133467 133469 133475 133481 133485 133487 133491 133497 133499 133505 133509 133511 133515 133517 133521 133523 133525 133526 133527 133529 133530 133531 133533 133535 133539 133541 133545 133547 133551 133557 133559 133565 133569 133571 133575 133581 133587 133589 133595 133599 133601 133607 133611 133617 133625 203614

 ),其反应类型是
),其反应类型是 有如下性质:
有如下性质: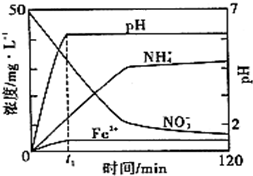 I.铁盐、亚铁盐是实验室常用的药品.
I.铁盐、亚铁盐是实验室常用的药品.