水电解的化学方程式为2H2O
2H2↑+O2↑,某同学电解一定量的水,制得8gH2,则该8gH2的物质的量为( )
| ||
| A、2mol | B、4mol |
| C、8mol | D、89.6mol |
下列说法正确的是( )
| A、海水中提取镁的过程中有用到硫酸 |
| B、工业炼铁中加入石灰石的目的是除去铁矿石中的杂质 |
| C、铁、铝常温下不能和浓硫酸、浓硝酸反应 |
| D、铝热反应特指铝与氧化铁的反应 |
下列离子方程式书写正确的是( )
| A、钠与水的反应:Na+H2O═Na++OH-+H2↑ |
| B、溴化亚铁溶液中滴加少量氯水:2 Br-+Cl2═Br2+2Cl- |
| C、碳酸氢钙溶液加入过量的氢氧化钙溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
| D、等体积同浓度NaHSO4、Ba(OH)2两溶液混合H++SO42-+Ba2++OH-═BaSO4↓+H2O |
短周期元素M、W、X、Y、Z在元素周期表中的位置如图所示,其中M、W、X的原子序数之和等于30.下列判断正确的是( )
| M | W | |
| X | Y | Z |
| A、M的氢化物与Z的氢化物反应所得产物的水溶液呈中性 |
| B、最高价氧化物的水化物的酸性H3XO4强于HMO3 |
| C、X与Z形成的所有化合物分子中,各原子均满足8电子稳定结构 |
| D、Y与Z的最高正化合价之和的数值等于13 |
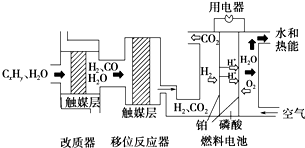 磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示.下列说法不正确的是( )
磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示.下列说法不正确的是( )| A、该系统中只存在化学能和电能的相互转化 | ||
B、在移位反应器中,反应CO(g)+H2O(g)
| ||
| C、改质器和移位反应器的作用是将CxHy转化为H2和CO2 | ||
| D、该电池正极的电极反应为O2+4H++4e-=2H2O |
下列各选项均有X、Y两种物质,将X缓缓滴入(通入)Y溶液中,无论X是否过量,均能用同一离子方程式表示的是( )
| X | Y | |
| A | 稀盐酸 | 碳酸钠溶液 |
| B | 偏铝酸钠溶液 | 硫酸溶液 |
| C | 硫化钠溶液 | 氯化铁溶液 |
| D | 一水合氨 | 氯化铝溶液 |
| A、A | B、B | C、C | D、D |
有一杯红褐色的透明液体,它可能是Fe(OH)3溶胶,为了证明它不是溶液而是胶体,可采用的最简单方法是( )
| A、丁达尔实验 | B、加入盐酸 |
| C、加热 | D、静置 |
用干燥的烧瓶集满一瓶氯化氢气体做喷泉实验,没有看到喷泉现象,下列哪种操作可能是导致实验失败的主要原因( )
| A、水中没有加石蕊 |
| B、装置的气密性不好 |
| C、烧瓶中收集的氯化氢较多 |
| D、连接烧瓶与烧杯的导管较短 |
在下列给定条件的溶液中,一定能大量共存的粒子组是( )
(1)无色溶液:S2-、Na+、ClO-、Cl-
(2)能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3-
(3)滴入KSCN溶液显血红色的溶液中:K+、Na+、SO42-、C6H5OH
(4)常温下,
=0.001mol?L-1的溶液:Na+、K+、SiO32-、NO3-
(5)K2S溶液中 SO42-、K+、Cl-、Cu2+
(6)水电离的c(H+)水=1.0×10-13mol?L-1溶液中 AlO2-、K+、SO42-、Br-
(7)pH=1的溶液:K+、Fe2+、I-、Br-
(8)与铝反应产生大量氢气的溶液:Na+、K+、NH4+、NO3-.
(1)无色溶液:S2-、Na+、ClO-、Cl-
(2)能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3-
(3)滴入KSCN溶液显血红色的溶液中:K+、Na+、SO42-、C6H5OH
(4)常温下,
| Kw |
| c(H+) |
(5)K2S溶液中 SO42-、K+、Cl-、Cu2+
(6)水电离的c(H+)水=1.0×10-13mol?L-1溶液中 AlO2-、K+、SO42-、Br-
(7)pH=1的溶液:K+、Fe2+、I-、Br-
(8)与铝反应产生大量氢气的溶液:Na+、K+、NH4+、NO3-.
| A、(2)(3)(4) |
| B、(4)(7) |
| C、(3)(4)(8) |
| D、(1)(5)(6) |
设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A、2.24LCO2中含有的原子数为0.3NA |
| B、0.1L3mol?L-1的NH4NO3溶液中含有的NH4+数目为0.3NA |
| C、5.6g铁粉与硝酸反应失去的电子数一定为0.3NA |
| D、4.5gSiO2晶体中含有的硅氧键数目为0.3NA |