下列实验式中,没有相对分子质量就可以确定分子式的是( )
①CH3 ②CH ③CH2 ④C2H5 ⑤CH2Cl2.
①CH3 ②CH ③CH2 ④C2H5 ⑤CH2Cl2.
| A、①② | B、③④⑤ |
| C、①④⑤ | D、①③④ |
在t℃时,10mL 0.4mol?L-1 H2O2溶液发生催化分解:2H2O2═2H2O+O2↑,不同时刻测得生成O2的体积(已折算为标准状况)如下表
下列叙述不正确的是(溶液体积变化忽略不计)( )
| t/min | 0 | 2 | 4 | 6 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 |
| A、0~2min H2O2平均反应速率比4~6min快 |
| B、0~6min的平均反应速率v(H2O2)≈3.3×10-2mol?L-1?min-1 |
| C、反应至6min时,c(H2O2)═0.3mol?L-1 |
| D、反应至6min时,H2O2分解了50% |
设NA代表阿伏加德罗常数,下列叙述正确的是( )
| A、标准状况下,11.2L的O2和NO的混合物含有的分子数约为0.5×6.02×1023 |
| B、1mol的羟基与1 mol的氢氧根离子所含电子数均为9 NA |
| C、常温常压下42g 乙烯和丁烯混合气体中,极性键数为6NA |
| D、6.4g SO2与足量氧气反应生成SO3,转移电子数为0.2NA |
常温下,0.1mol/L某一元酸(HA)溶液中
=1×10-8,下列叙述正确的是( )
| c(OH-) |
| c(H+) |
| A、溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH-)均增大 |
| B、溶液中水电离出的c(H+)=10-10mol/L |
| C、溶液中c(H+)+c(A-)=0.1 mol/L |
| D、与0.05mol/LNaOH溶液等体积混合后所得溶液中离子浓度大小关系为:c(A-)>c(Na+)>c(OH-)>c(H+) |
在密闭容器中进行X2(g)+4Y2(g)?2Z2(g)+3Q2(g)的反应,其中X2、Y2、Z2、Q2的起始浓度分别为:0.1mol/L、0.4mol/L、0.2mol/L、0.3mol/L,反应达到平衡,各物质的浓度不可能为( )
| A、c(X2)=0.15 mol/L |
| B、c(Y2)=0.9 mol/L |
| C、c(Z2)=0.3 mol/L |
| D、c(Q2)=0.6 mol/L |
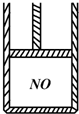 如图为装有活塞(质量忽略不计)的密闭容器,内盛22.4mL一氧化氮,若通入11.2mL氧气(气体体积均在标准状况下测定),保持温度压强不变,则容器内的密度为(提示:不考虑NO转化为NO2的可逆性)( )
如图为装有活塞(质量忽略不计)的密闭容器,内盛22.4mL一氧化氮,若通入11.2mL氧气(气体体积均在标准状况下测定),保持温度压强不变,则容器内的密度为(提示:不考虑NO转化为NO2的可逆性)( )| A、等于1.369g?L-1 |
| B、等于2.054g?L-1 |
| C、在1.369g?L-1和2.054g?L-1之间 |
| D、在2.054g?L-1和4.108g?L-1之间 |
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )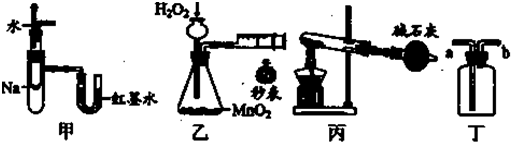

| A、装置甲可用于验证反应的热效应 |
| B、装置乙可定量测定化学反应的速率 |
| C、装置丙可用于实验室以NH4Cl为原料制备少量NH3 |
| D、装置丁a口进气可收集NH3、C12等气体 |
如图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )


| A、电负性:X>Y>Z |
| B、气态氢化物的稳定性及其水溶液的酸性:R>W |
| C、W、X形成的化合物以及它们与水反应生成物都是共价化合物 |
| D、Y、Z、W的最高价氧化物对应的水化物两两之间都能发生反应 |
下列变化属于吸热反应的是( )
| A、浓硫酸稀释 |
| B、液态水汽化 |
| C、生石灰跟水反应生成熟石灰 |
| D、将胆矾加热变为白色粉末 |