下列有关实验操作的叙述正确的是( )
| A、用量筒取5.00mL 1.00mol/L盐酸于50mL容量瓶中,加水稀释至刻度,可配制0.100mol/L盐酸 |
| B、将固体加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的溶液 |
| C、用10mL质量分数为98%的H2SO4,用水稀释至100mL,H2SO4的质量分数为9.8% |
| D、质量分数为10%的氨水与质量分数为20%的氨水等体积混合,所得氨水的质量分数小于15% |
下列装置或操作能达到实验目的是( )
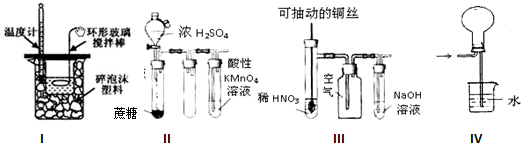

| A、实验I:中和热测定 |
| B、实验II:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |
| C、实验III:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
| D、实验IV:可用于HCl气体的吸收 |
下列实验操作或方法中,不正确的是( )
A、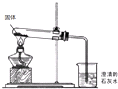 区别碳酸钠和碳酸氢钠 |
B、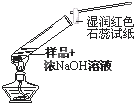 检验试液中NH4+的存在 |
C、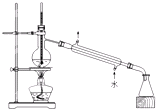 实验室蒸馏石油 |
D、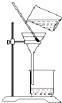 过滤操作 |
配制物质的量的浓度的溶液,造成浓度偏高的操作是( )
| A、定容后,又重新加水至刻度线 |
| B、烧杯和玻璃棒的溶液未转入容量瓶中 |
| C、定容时,眼睛俯视刻度线 |
| D、容量瓶洗净后没有干燥 |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、27 g Al在标准状况下的22.4 L Cl2中燃烧,转移的电子总数为3NA |
| B、1 mol明矾与水完全反应转化为氢氧化铝胶体后,其中胶体粒子的数目为NA |
| C、标准状况下,分子数为NA的N2、C2H4混合气体的质量无法确定 |
| D、铁铝混合物与一定量盐酸反应生成1 mol H2时,转移电子数是2NA |
实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的是( )
A、 实验室中制取少量蒸馏水 |
B、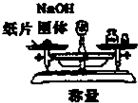 城区一定质量的NaOH固体 |
C、 用滴瓶长期保存NaOH溶液 |
D、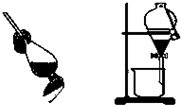 除去乙醇中溶有的少量水 |
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、7gCnH2n中含有的氢原子数目为NA |
| B、18gD2O中含有的质子数目为10NA |
| C、标准状况下,22.4LCHCl3中含有氯原子数目为3NA |
| D、1 L0.5mol/LNa2CO3 溶液中含有的CO32-数目为0.5NA |
已知某温度下蒸馏水中的c(H+)=1×10-6mol/L,在此温度下将乙酸和氢氧化钠溶液混合,所得溶液的pH=7,此溶液中( )
| A、c(CH3COO-)>c(Na+) |
| B、c(CH3COO-)<c(Na+) |
| C、c(CH3C+OO-)=c(Na+) |
| D、无法确定c(CH3COO-)与c(Na+)的关系 |
根据你的生活经验和所学的科学知识,判断下列做法正确的是( )
| A、用钢丝球洗涮铝锅 |
| B、用活性炭除去冰箱里的异味 |
| C、室内烤火放一盆水,防止CO中毒 |
| D、用水浇灭着火的油锅 |