下列实验操作正确的是( )
| A、用CCl4萃取碘水中的碘,上层的水从分液漏斗的下端放出 |
| B、配制溶液时,摇匀后发现液面低于刻度,再加水至刻度线 |
| C、把溶液从烧杯中转移到容量瓶时用玻璃棒引流 |
| D、称量时,托盘天平的左盘放砝码,右盘放称量药品 |
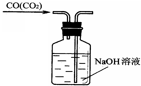
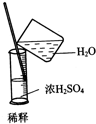
下列装置所示的实验中,能达到实验目的是( )
A、 分离碘和酒精 |
B、 除去Cl2中的HCl |
C、 排水法收集NO |
D、 配制硫酸溶液 |
乙醇分子所含官能团的名称是( )
| A、乙氧基 | B、羟基 | C、乙基 | D、甲基 |
下列离子方程式书写正确的是( )
| A、NH4HCO3溶液与过量的NaOH溶液反应:NH4++OH-=NH3↑+H2O |
| B、从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
| C、铜片插入氯化铁溶液中:2Fe3++Cu=2Fe2++Cu2+ |
| D、Cl2通入水中:Cl2+H2O=2H++Cl-+ClO- |
下列说法中,不正确的是( )
| A、大多数有机物难溶于水,易溶于汽油、苯等有机溶剂 |
| B、有机物的熔点低 |
| C、有机物都是非电解质,不易导电 |
| D、有机物的化学反应比较复杂,一般较慢,且常伴有副反应发生 |
下列关于催化剂的叙述正确的是( )
| A、催化剂不参加化学反应 |
| B、催化剂可以使原本不能发生的反应得以发生 |
| C、催化剂只降低正反应的活化能 |
| D、催化剂能够增大活化分子的百分数 |
0.1mol/L的亚硫酸钠溶液15mL,恰好将1×10-3mol的XO4-离子还原,则X在还原产物中的化合价是( ) 价.
| A、+1 | B、+2 | C、+3 | D、+4 |
有一处于平衡状态的反应:X(s)+3Y(g)?3Z(g),△H<0,为了使平衡向生成Z的方向移动,应选择的条件是( )
①加入X②低温③高压④低压⑤加催化剂⑥分离出Z.
①加入X②低温③高压④低压⑤加催化剂⑥分离出Z.
| A、①③⑤ | B、②③⑤ |
| C、②⑥ | D、②④⑥ |
已知 25℃时有关弱酸的电离平衡常数:
下列有关说法正确的是( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A、NaHCO3溶液中,一定有c(Na+)=c(HCO3-)+c(CO32-) |
| B、1 mol?L-1HCN溶液与1mol?L-1NaOH溶液等体积混合后,测得所得溶液显酸性 |
| C、等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(NaHCO3)>pH(CH3COONa) |
| D、1 mol?L-1醋酸溶液加水稀释,所有离子浓度均减小 |