将3mol 甲烷与氯气发生取代反应,待反应完全后测知四种取代物的物质的量相同,测消耗的氯气有( )
| A、2mol | B、10mol |
| C、7.5mol | D、6mol |
在一密闭容器中,反应aA(g)?bB(g)达平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的45%,则( )
| A、平衡向正反应方向移动了 |
| B、物质A的转化率减小了 |
| C、物质B的质量分数增大了 |
| D、a>b |
要除去下列四种物质中的少量杂质(括号内的物质为杂质):甲:CaCO3(Na2CO3);乙:NaOH(Na2CO3);丙:KCl(KHCO3);丁:碳粉(CuO)可选用的试剂及操作方法有:①加适量盐酸,搅拌,过滤;②加适量水,搅拌,过滤;③加适量盐酸,蒸发;④溶解,加适量石灰水,过滤,蒸发.下列组合正确的是( )
| A、甲-②,乙-④ |
| B、乙-③,丙-① |
| C、丙-①,丁-② |
| D、丁-①,丙-③ |
用NA表示阿伏伽德罗常数的值.下列叙述正确的是( )
| A、1mol硝基(-NO2)与NA个二氧化氮气体分子所含电子数相等 |
| B、1mol氢氧根离子(OH-)与NA个羟基(-OH)所含电子数相等 |
| C、在相同温度下,pH=1且体积为1L的硫酸溶液所含氢离子数与pH=13且体积为1L的氢氧化钠溶液所含氢氧根离子数一定均为0.1NA |
| D、在反应2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑中,每生成1molO2该反应共转移的电子数为6NA |
对于化学反应A+B=C+D的下列说法中,正确的是( )
| A、若C、D分别为单质和化合物,则该反应一定是置换反应 |
| B、若C、D分别为盐和水,则该反应一定是中和反应 |
| C、若A、B、C、D都是化合物,该反应一定是复分解反应 |
| D、若A为碱溶液,B为盐溶液,则C和D可能是两种沉淀 |
已知25℃时,电离常数K1(H 2CO3)>K(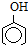 )>K2(H 2CO3),且知苯甲酸酸性比碳酸强,水杨酸(
)>K2(H 2CO3),且知苯甲酸酸性比碳酸强,水杨酸(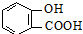 )与碳酸钠溶液反应生成CO2的同时,不能生成的物质是( )
)与碳酸钠溶液反应生成CO2的同时,不能生成的物质是( )
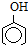 )>K2(H 2CO3),且知苯甲酸酸性比碳酸强,水杨酸(
)>K2(H 2CO3),且知苯甲酸酸性比碳酸强,水杨酸(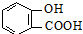 )与碳酸钠溶液反应生成CO2的同时,不能生成的物质是( )
)与碳酸钠溶液反应生成CO2的同时,不能生成的物质是( )A、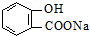 |
| B、NaHCO3 |
C、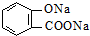 |
| D、H2O |
甲酸溶液中存在电离平衡HCOOH?H++HCOO-,下列叙述正确的是( )
| A、甲酸溶液中离子浓度的关系满足c(H+)=c(OH-)+c(HCOO-) |
| B、0.10mol/L的HCOOH溶液中加NaCl溶液,溶液中c(OH-)减小 |
| C、其他条件不改变的情况下HCOOH溶液中加少量的HCOONa固体,平衡逆向移动电离常数变小 |
| D、其他条件不改变的情况下升高温度HCOOH溶液的pH变大 |
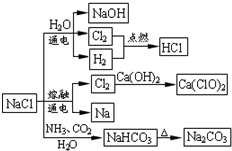 NaCl是一种化工原料,可以制备一系列物质(如图所示).下列说法正确的是( )
NaCl是一种化工原料,可以制备一系列物质(如图所示).下列说法正确的是( )| A、常温下干燥Cl2能用钢瓶贮运,所以Cl2与铁不反应 |
| B、25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| C、源石灰乳与Cl2的反应中Cl2既是氧化剂,又是还原剂 |
| D、图中所示转化反应都是氧化还原反应 |
常温下有体积相同的四种溶液:①pH=3的CH3COOH溶液;②pH=3的HCl溶液;③pH=11的氨水;④pH=11的NaOH溶液.下列说法正确的是( )
| A、①与②中c(H+)相同 |
| B、①与④混合,溶液中c(CH3COO-)=c(Na+) |
| C、②和③混合,所得混合溶液的pH等于7 |
| D、③与④分别用等浓度的盐酸中和,消耗盐酸的体积相同 |
常温下,下列有关叙述正确的是学( )
| A、NaB溶液的pH=8,c(Na+)-c(B-)=0.99×10-6mol/L |
| B、Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、c(NH4+)=c(Cl-)的NH4Cl和氨水的混合溶液,其pH可能等于或大于7 |
| D、10 mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积(假设混合后的体积是两溶液体积之和)V(总)≥20mL |