下列有关摩尔的使用正确的是( )
| A、1mol O的质量为16g?mol-1 |
| B、0.5mol He约含有6.02×1023个电子 |
| C、2H既表示2个氢原子又表示2mol氢原子 |
| D、每摩尔微粒均含有6.02×1023个原子 |
一元中强酸次磷酸(H3PO2)是一种精细化工产品,下列说法正确的是( )
| A、次磷酸的电离方程式为H3PO2?3H++PO23- |
| B、次磷酸中P的化合价为+1 |
| C、NaH2PO2是酸式盐 |
| D、NaH2PO2溶液显弱酸性 |
目前市场上的手提应急灯,主要用的是“无液干粉”铅酸蓄电池,其原理是将强腐蚀性的浓硫酸灌注到硅胶中,使电解质溶液不易发生泄漏,大大改善了电池的性能.所用的原料仍然是Pb-PbO2-H2SO4,下列关于该铅酸蓄电池的说法正确的是( )
| A、充电时,电源的正极接蓄电池标“+”的一极,电池上标有“-”的一极发生氧化反应 |
| B、“无液干粉”铅酸蓄电池彻底改变了原来的铅酸蓄电池的原理 |
| C、放电时,在铅酸蓄电池的负极发生还原反应 |
| D、若用此铅酸蓄电池电解饱和NaCl溶液,标准状况下制备1.12LCl2,电池内至少消耗H2SO40.10 mol |
对于实验的描述正确的是( )
A、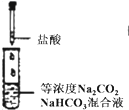 逐滴滴加稀盐酸时,试管中立即产生大量气泡 |
B、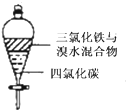 充分振荡后静置,下层溶液为橙红色,上层无色 |
C、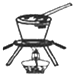 从饱和食盐水中提取NaCl晶体 |
D、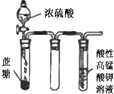 酸性KMnO4溶液中有气泡出现,且溶液颜色逐渐变浅乃至褪去 |
设NA代表阿伏加德罗常数的数值,下列说法不正确的是( )
| A、36g镁在足量的二氧化碳气体中完全燃烧共转移的电子数为3NA |
| B、1L 1mol?L-1的Na2CO3溶液中含有Na+的数目为NA |
| C、标准状况下,2.24L CO2和SO2混合气体中含有的氧原子数目为0.2NA |
| D、常温常压下,Na2O2与足量H2O反应,共生成0.2mol O2,转移电子的数目为0.4NA |
使一定质量的锌与100mL18.5mol/L浓H2SO4充分反应,锌完全溶解,同时生成气体A 33.6L(标准状况下).将反应后的溶液稀释至1L,测得溶液c(H+)为0.1mol/L,往反应后的溶液中加入足量的BaCl2溶液,会生成的BaSO4沉淀,以下说法中不正确的是( )
| A、生成的SO2气体为0.3mol |
| B、生成的SO2气体为1.5mol |
| C、生成的H2气体为1.2mol |
| D、生成的BaSO4沉淀361.15g |
从碘水中提取碘可供选择的试剂是( )
| A、苯、酒精 |
| B、汽油、酒精 |
| C、汽油、乙酸 |
| D、四氯化碳、苯 |
已知反应:
2FeCl3+2KI═2FeCl2+2KCl+I2;
2FeCl2+Cl2═2FeCl3;
I2+SO2+2H2O═H2SO4+2HI;
下列物质的氧化性由强到弱的顺序是( )
2FeCl3+2KI═2FeCl2+2KCl+I2;
2FeCl2+Cl2═2FeCl3;
I2+SO2+2H2O═H2SO4+2HI;
下列物质的氧化性由强到弱的顺序是( )
| A、FeCl3>I2>Cl2>H2SO4 |
| B、FeCl2>FeCl3>Cl2>I2 |
| C、Cl2>FeCl3>I2>H2SO4 |
| D、Cl2>H2SO4>I2>FeCl3 |
下列物质中,能导电且为电解质的是( )
| A、熔融态的NaC1 | B、固体NaOH |
| C、铁 | D、稀硫酸 |