Fe(OH)3胶体稳定存在的主要原因是( )
| A、胶粒直径小于1nm |
| B、胶粒做布朗运动 |
| C、胶粒带正电荷 |
| D、胶粒不能透过半透膜 |
相同温度下,体积为2L的两个恒容容器中发生:N2+3H2?2NH3△H=-92.6KJ/mol(均为气态物质)有下表所示实验数据:下列有关说法正确的是( )
| 容器编号 | 起始时各物质的物质的量/mol | 达到平衡时体系能量的变化/KJ | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 46.3 |
| ② | 0 | 0 | 2 | Q1>0 |
| ③ | 0.3 | 0.9 | 1.4 | Q2>0 |
| A、Q1=Q2=46.3KJ |
| B、②中NH3的转化率大于③中NH3的转化率 |
| C、容器 ①与③分别达到平衡时,平衡常数相同,且K<1 |
| D、将容器 ①的反应条件换为恒温恒压中进行(投料量不变),达到平衡时,气体平均摩尔质量较恒温恒容时减小了 |
钢材可以用作桥梁的结构材料,是因为它( )
| A、有良好的导热性 |
| B、有一定的机械强度 |
| C、不易受空气和水的作用 |
| D、有良好的导电性 |
下列有关说法中,错误的是( )
| A、若NA表示阿伏加德罗常数的值,则标准状况下11.2 L H2所含氢原子数为NA |
| B、1 L 1 mol?L-1的氯化钙溶液中,Cl-的浓度为2 mol/L |
| C、硫酸的摩尔质量为98g |
| D、从 1 mol?L-1的NaCl溶液中倒出5 mL溶液,Na+的浓度为1 mol?L-1 |
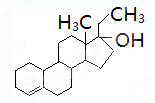 为实现2008北京“科技奥运”战略,我国兴奋剂检测生物芯片装置已定型和批量生产,可快捷检测常见的l6种兴奋剂.已知某兴奋剂乙基雌烯醇(etylestrenol)的结构如图所示.下列叙述中正确的是( )
为实现2008北京“科技奥运”战略,我国兴奋剂检测生物芯片装置已定型和批量生产,可快捷检测常见的l6种兴奋剂.已知某兴奋剂乙基雌烯醇(etylestrenol)的结构如图所示.下列叙述中正确的是( )| A、该物质可以视为酚类 |
| B、在浓硫酸作用下,分子内消去一个水分子只生成一种有机产物 |
| C、能使溴的四氯化碳溶液褪色 |
| D、该物质分子中的所有碳原子均共面 |
下列变化或数据与氢键无关的是( )
| A、水的沸点比硫化氢的沸点高 |
| B、氨分子易溶于水 |
| C、冰可以浮在水面上 |
| D、H2O是一种非常稳定的化合物 |
“天宫一号”飞行器在太空工作期间必须有源源不断的电源供应.其供电原理是:白天太阳能帆板发电,将一部分电量直接供给天宫一号,另一部分电量储存在镍氢电池里,供黑夜时使用.镍氢电池放电时的总反应为:MH+NiO(OH)═M+Ni(OH)2(M为氢化物电极的储氢金属,也可看作H2直接参加反应).下列说法正确的是( )
| A、充电时阴极区电解质溶液pH减小 |
| B、在使用过程中此电池要不断补充水 |
| C、放电时NiO(OH)在电极上发生氧化反应 |
| D、充电时阳极反应为Ni(OH)2-e-+OH-═NiO(OH)+H2O |
下列实验操作正确的是( )
| A、用托盘天平称量4.00g氢氧化钠固体 |
| B、用10mL量筒量取8.5mL蒸馏水 |
| C、用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 |
| D、用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH |
我国镍氢电池居世界先进水平,我军潜艇将装备国产大功率镍氢动力电池.常见镍氢电池的某极是储氢合金LaNi5H6 (LaNi5H6中各元素化合价均为零),电池反应通常表示为:LaNi5H6+6NiO(OH)
LaNi5+6Ni(OH)2,下列说法正确的是( )
| 放电 |
| 充电 |
| A、充电时储氢合金作阳极 |
| B、放电时每转移6mol电子,有6mol NiO(OH)被氧化 |
| C、充电时阳极周围PH增大 |
| D、放电时负极反应:LaNi5H6+6OH--6e-═LaNi5+6H2O |
某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是( )
| A、K+、Na+、HSO3-、NO3- |
| B、Na+、ClO-、SO42-、Cl- |
| C、NH4+、K+、SO42-、F- |
| D、Ag+、Na+、NO3-、CH3COOO- |