下列关于摩尔质量的叙述正确的是( )
| A、1molH2SO4的质量是98g/mol |
| B、CO2的摩尔质量等于CO2的相对分子质量 |
| C、1mol任何物质的质量等于该物质的相对分子质量 |
| D、Na的摩尔质量是23g/mol |
下列各项叙述中不正确的是( )
| A、10℃时NaCl溶解度为35.7g,则此时饱和NaCl 溶液的质量分数小于35.7% |
| B、向Na2CO3溶液中加入少量NaHCO3 固体,溶液pH 减小 |
| C、50mL1.0mol?L-1盐酸与60mL 1.0 mol?L-1盐酸分别跟50mL 1.1mol?L-1NaOH溶液进行反应,中和热数值不相等 |
| D、一定条件下,向水中加入少量NaHSO4,可使水的电离程度减小 |
在其它条件不变时,10℃时以某物质表示的反应速率为3mol/(L?s),已知温度每升高10℃反应速率是原来的2倍,则温度为50℃时,该反应的速率为( )
| A、48 mol/(L?s) |
| B、36mol/(L?s) |
| C、24 mol/(L?s) |
| D、12 mol/(L?s) |
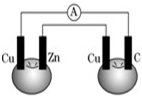 如图所示,铜片、锌片和石墨棒用导线连接后插入番茄里,电流计中有电流通过,则下列说法正确的是( )
如图所示,铜片、锌片和石墨棒用导线连接后插入番茄里,电流计中有电流通过,则下列说法正确的是( )| A、锌片是负极 |
| B、两个铜片上都发生氧化反应 |
| C、石墨是阳极 |
| D、两个蕃茄都形成原电池 |
下列事实不能用勒夏特列原理来解释的是( )
| A、加压有利于SO2与O2反应生成SO3 |
| B、用过量空气煅烧硫铁矿可以提高原料的利用率 |
| C、加入催化剂都能使合成氨的反应速率加快 |
| D、温度过高对合成氨反应不利 |
将Na2O2逐渐加入到含有H+、Mg2+、Al3+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入的Na2O2物质的量(mol)的关系如图所示,则原溶液中的Mg2+、Al3+、NH4+物质的量分别( )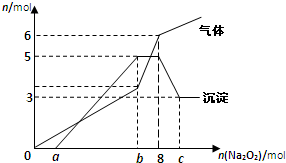

| A、2 mol、3 mol、6 mol |
| B、3 mol、2 mol、6mol |
| C、2 mol、3 mol、4 mol |
| D、3 mol、2 mol、2 mol |
除去下列物质中少量杂质的方法不正确的是( )
| A、除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤 |
| B、除去CO2中混有的HCl:用饱和NaHCO3溶液洗气 |
| C、除去BaCO3固体中混有的BaSO4:加入过量的盐酸、过滤、洗涤 |
| D、除去乙炔中混有的少量H2S、PH3:通过CuSO4溶液后,洗气 |
下列实验原理正确的是( )
| A、定性检验SO32-时,将BaCl2溶液用稀HNO3酸化 |
| B、为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液酸化 |
| C、为得到MgCl2固体,将MgCl2溶液加热蒸干即可 |
| D、用酚酞试液可鉴别饱和食盐水和饱和纯碱溶液 |
下列离子方程式不正确的是( )
| A、4mol/L的NaAlO2溶液和7mol/L的HCl等体积互相混合均匀4AlO2-+7H++H2O=3Al(OH)3↓+Al3+ |
| B、向100mL0.1mol/L的碳酸钠溶液中逐滴加入0.1mol/L CH3COOH:CO32-+CH3COOH=CO2↑+2CH3COO-+H2O |
| C、向硫酸铝铵溶液中滴加过量的氢氧化钡溶液:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3?H2O+2H2O |
| D、KHS的水解:HS-+H2O?H2S+OH- |
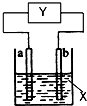 如图装置中a为纯铜棒,Y为电路的未知部分,X为某种液体,下列说法正确的是( )
如图装置中a为纯铜棒,Y为电路的未知部分,X为某种液体,下列说法正确的是( )