下列关于实验操作的陈述中正确的是( )
| A、用规格为20mL的量筒一次量取16mL溶液,比用规格为10mL的量筒分两次量取16mL溶液的误差小 |
| B、蒸发时,当有大量晶体析出即停止加热,利用余热蒸干 |
| C、过滤时,为了加速溶液透过滤纸,可以用玻璃棒末端轻轻搅拌滤纸上的混合物 |
| D、配制一定物质的量浓度溶液时,为了避免溶质的损失,直接把称量的固体溶质转移到容量瓶中 |
下列事实与胶体性质无关的是( )
| A、水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染 |
| B、一束平行光线射入氢氧化铁胶体里,从侧面可以看到一条光亮的通路 |
| C、将植物油倒入水中用力搅拌形成油水混合物 |
| D、氢氧化铁胶体中滴入稀硫酸,先看到红褐色沉淀生成而后沉淀溶解 |
下列有关试剂的保存方法,错误的是( )
| A、铝片直接放置在空气中 |
| B、漂白粉保存在烧杯中 |
| C、新制的氯水通常保存在棕色细口玻璃试剂瓶中 |
| D、氢氧化钠溶液用带橡胶塞的试剂瓶贮存 |
维生素A对人的视力有非常重要的作用,其结构简式如图,下列关于该化合物的说法中,正确的是( )
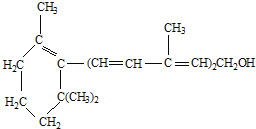
①维生素A是一种不饱和的一元醇;
②维生素A含有苯环结构;
③维生素A含有两种官能团;
④维生素A的一个分子中含有3个双键.

①维生素A是一种不饱和的一元醇;
②维生素A含有苯环结构;
③维生素A含有两种官能团;
④维生素A的一个分子中含有3个双键.
| A、②④ | B、①③ |
| C、③④ | D、全部正确 |
下列各组分子中,都属于含极性键的非极性分子的是( )
| A、CO2 H2S |
| B、C2H4 CH4 |
| C、C60 C2H4 |
| D、NH3 HCl |
向100mL a mol/L的AlCl3溶液中加入金属钾,完全反应后恰好只形成KCl和KAlO2的溶液,则加入钾的物质的量为( )
| A、0.1a mol |
| B、0.4a mol |
| C、0.3a mol |
| D、a mol |
下列说法中正确的是( )
| A、在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
| B、生成物全部化学键形成时所释放的能量大于破坏反应物全部化学键所吸收的能量时,反应为吸热反应 |
| C、反应产物的总能量大于反应物的总能量时,△H>0 |
| D、△H的大小与热化学方程式的计量系数无关 |
如列图象及对应说法正确的是( )


| A、图1表示恒温恒压下条件,向2HI?H2+I2△H>0的反应达到平衡的容器中充入HI,甲表示正反应速率,乙表示逆反应速率 |
| B、图1表示恒容下条件,向2HI?H2+I2△H>0的反应达到平衡的容器加热,甲表示正反应速率,乙表示逆反应速率 |
| C、图2表示恒温条件下,压缩2SO3(g)?2SO2(g)+O2(g)△H>0平衡反应体系,甲表示的SO3物质的量的变化,乙表示的SO3物质的量浓度的变化 |
| D、图2表示恒容条件下,对于2SO3(g)?2SO2(g)+O2(g)△H>0反应平衡体系,甲表示升高温度SO3物质的量的变化,乙表示增加O2后SO3物质的量变化 |
美国斯坦福大学研究人员发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为5MnO2+2Ag+2NaCl═Na2Mn5O10+2AgCl.下列有关“水”电池在海水中放电时的说法正确的是( )
| A、负极反应式:Ag+Cl-+e-═AgCl |
| B、电池的正极用二氧化锰纳米棒为材料,可大大提高发电效率 |
| C、Na+不断向“水”电池的负极移动 |
| D、每转移2 mol电子,正极就有5 mol MnO2被氧化 |
常温下,下列各组离子或分子在指定溶液中能大量共存的是( )
A、使甲基橙呈红色的溶液中:MnO4-、Al3+、C2H5OH、SO
| ||||
| B、水电离出的(H+)=1×10-14 mol?L-1的溶液中:Na+、NH4+、Cl-、SiO32- | ||||
| C、c (NaHCO3)=0.1 mol?L-1 的溶液中:K+、C6H5O-、SO42-、CO32- | ||||
D、c(H+)/c(OH-)=1012的溶液中:NH
|