因发生电极反应,直接破坏了该电极附近水的电离平衡的是.( )
| A、用惰性电极电解氯化铜溶液的阴极 |
| B、铜锌(稀硫酸作电解质)原电池的正极 |
| C、用惰性电极电解饱和食盐水的阴极 |
| D、用惰性电极电解饱和硫酸钠溶液的阳极 |
设NA代表阿伏加德罗常数,下列说法正确的是( )
| A、5.6 g铁与过量盐酸反应转移的电子数为0.3NA |
| B、常温下,10ml1mol/LNa2CO3溶液中阴离子总数大于0.01NA |
| C、标准状况下,22.4 L氦气与22.4 L氢气所含原子数均为2NA |
| D、30gSiO2中含Si-O键数目为NA |
下列实验中,能达到预期目的是( )
| A、用过滤法除去Fe(OH)3胶体中的FeCl3 |
| B、为鉴别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量 |
| C、向某溶液中滴入BaCl2溶液和稀HNO3,来检验溶液中是否含有SO42- |
| D、将Na投入到CuSO4溶液中置换出铜,来证明钠的金属性比铜强 |
关于下列各装置图的叙述中,不正确的是( )
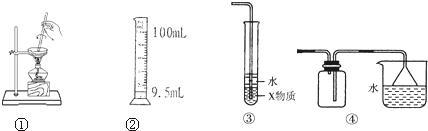

| A、装置①是把饱和食盐水中的食盐提取出来 |
| B、装置②用100mL量筒量取9.5mL液体 |
| C、装置③中X若为CCl4,可用于吸收NH3或HCl,并可防止倒吸 |
| D、装置④可用于收集NH3,并吸收多余的NH3 |
下列反应的离子方程式正确的是( )
| A、氯气通人含等物质的量的FeBr2溶液中:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2 |
| B、澄清石灰水与少量的碳酸氢钠溶液反应:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O |
| C、铜与浓硝酸反应:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O |
| D、硫酸氢钠溶液滴入Ba(OH)2溶液至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
向含n mol 硫酸铝的溶液中加入m mol NaOH溶液,观察到的现象是先有白色沉淀生成,后部分溶解,则生成Al(OH)3沉淀的物质的量是( )
| A、(8n-m)mol |
| B、(4m-n)mol |
| C、(4n-m)mol |
| D、(7n-m)mol |
构造原理揭示的电子排布能级顺序,实质是各能级能量高低.若以E(nl)表示某能级的能量,以下各式中正确的是( )
| A、E(4s)>E(3s)>E(2s)>E(1s) |
| B、E(4s)>E(3d)>E(3p)>E(3s) |
| C、E(5s)>E(4f)>E(4s)>E(3d) |
| D、E(5s)>E(4s)>E(4f)>E(3d) |
下列反应中,氧化剂与还原剂物质的量的关系为1:2的是( )
| A、4KI+O2+2H2O═4KOH+2I2 | ||||
| B、2CH3COOH+Ca(ClO)2═2HClO+Ca(CH3COO)2 | ||||
| C、I2+2NaClO3═2NaIO3+Cl2 | ||||
D、MnO2+4HCl
|
控制适当的条件,将反应Fe3++Ag═Fe2++Ag+设计成如图所示的原电池.下列判断正确的是( )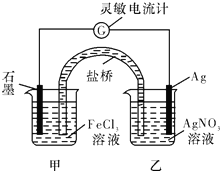

| A、反应开始时,石墨棒作阳极,银棒作阴极 |
| B、灵敏电流计的读数由小变大,再变小 |
| C、反应达化学平衡时,电流计读数最大 |
| D、反应达化学平衡时,在乙烧杯中滴入一定量的NaCl溶液,电流计指针又偏转 |
由1-丙醇制取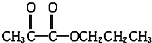 ,最简便的流程需要下列反应的顺序应是( )
,最简便的流程需要下列反应的顺序应是( )
a.氧化 b.还原 c.取代 d.加成 e.消去 f.中和 g.加聚 h.酯化.
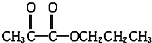 ,最简便的流程需要下列反应的顺序应是( )
,最简便的流程需要下列反应的顺序应是( )a.氧化 b.还原 c.取代 d.加成 e.消去 f.中和 g.加聚 h.酯化.
| A、e、d、c、a、h |
| B、b、d、f、g、h |
| C、a、e、d、c、h |
| D、b、a、e、c、f |