下列反应属于放热反应的是( )
A、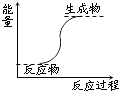 能量变化如图所示的反应 |
| B、燃烧反应和铝热反应 |
| C、化学键断裂吸收的热量比化学键生成放出的热量多的反应 |
| D、氢氧化钡晶体和氯化铵晶体的反应 |
下列物质不能用来制O2的是( )
| A、Na2O |
| B、Na2O2 |
| C、KMnO4 |
| D、KClO3 |
下列除杂(括号内为杂质)所选用的试剂及操作方法均正确的一组是( )
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | NaOH(Na2CO3) | 盐酸 | - |
| B | FeCl2(FeCl3) | 铜粉 | 过滤 |
| C | Mg(Al) | 氢氧化钠溶液 | 过滤 |
| D | CO2(HCl) | Na2CO3溶液 | 洗气 |
| A、A | B、B | C、C | D、D |
绿色化学又称环境友好化学,他的主要特点之一是:提高原子的利用率,使原料中所有的原子全部转化到产品中,实现“零排放”.下列反应符合绿色化学这一特点的是( )
A、工业冶铁 Fe2O3+3CO
| ||||
| B、用生石灰制熟石灰 CaO+H2O═Ca(OH)2 | ||||
| C、实验室制二氧化碳2HCl+CaCO3═CaCl2+H2O+CO2↑ | ||||
| D、实验室制氢气 Zn+H2SO4═ZnSO4+H2↑ |
下列说法不正确的是( )
| A、元素分析仪可同时对有机物中碳、氢、氧、硫等多种元素进行分析,其特点是样品量少,速度快 |
| B、1H核磁共振谱能反映出有机物中不同环境氢原子的种数和个数 |
| C、根据红外光谱图的分析可以初步判断有机物中具有哪些基团 |
| D、同位素示踪法可以用来确定有机反应中化学键的断裂位置 |
已知铅+2价稳定,+4价铅有很强的氧化性,今有6种下列物质:H2O、PbO2、Pb(NO3)2、HMnO4、HNO3和Mn(NO3)2组成一个化学方程式.下列有关说法正确的是( )
| A、反应物中发生氧化反应的物质PbO2 |
| B、被还原的元素是Mn(NO3)2中Mn |
| C、反应中1mol氧化剂得到5mol电子 |
| D、请将反应物配平后的PbO2与Mn(NO3)2系数之比5:2 |
下列实验操作中,正确的是( )
| A、蒸发溶液时,边加热加搅拌,直至蒸发皿内的液体蒸干 |
| B、量取25.00LKMnO4溶液时,应选择酸式滴定管 |
| C、配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4注入容量瓶中加水稀释,边注入边搅拌 |
| D、配制一定物质的量浓度的溶液时,若未洗涤烧杯和玻璃棒,则会导致所配溶液的物质的量浓度偏高 |
下列各组中两种物质在溶液里的反应,可用同一离子方程式表示的是( )
| A、KCl+AgNO3;AlCl3+AgNO3 |
| B、NaHCO3+H2SO4;Na2CO3+HCl |
| C、NaHCO3+NaOH;Ca(HCO3)2+KOH |
| D、BaCl2+H2SO4;Ba(OH)2+H2SO4 |
下列热化学方程式中△H表示可燃物燃烧热的是( )
A、C(s)+
| ||
| B、2H2(g)+O2(g)═2H2O(g)△H═-571.6kJ/mol | ||
| C、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H═-802.3kJ/mol | ||
| D、C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(I)△H═-2800kJ/mol |
关于下列图示的说法不正确的是( )
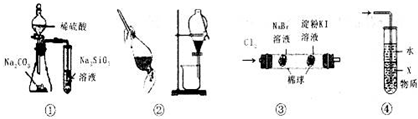

| A、图①所示实验,能比较硫、碳、硅三种元素的非金属性强弱 |
| B、装置②可用于从溴水中提取单质溴 |
| C、装置③中,左边棉花变为橙色,右边棉花变为蓝色,证明氧化性:Cl2>Br2>I2 |
| D、装置④中,X若为CCl4,可用吸收NH3或HCl,并防止倒吸 |