根据相关的化学原理,下列判断正确的是( )
| A、由于水中存在氢键,所以稳定性:H2O>H2S |
| B、由于非金属性F>Cl>Br>I,所以酸性:HF>HCl>HBr>HI |
| C、分散质粒子直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| D、若R2-和M+的电子层结构相同,则原子半径 R>M |
下列物质中,在题中所给状态下能够导电的电解质是( )
| A、铜丝 | B、熔融的氯化镁 |
| C、氯化钠固体 | D、蔗糖溶液 |
化学无处不在,下列与化学有关的说法,正确的是( )
| A、纤维素在人体内可水解为葡萄糖,故可作人类的营养物质 |
| B、侯氏制碱法的工艺过程中应用了物质溶解度的差异 |
| C、碘是人体必须微量元素,所以要多多吃富含高碘酸的食物 |
| D、氯化铝是一种电解质,可用于电解法制铝 |
有一块粗铝,含有铁和硅两种杂质.取两份等质量的样品分别放入足量的稀硫酸和足量的稀氢氧化钠溶液中,放出等质量的H2,则该粗铝中铁和硅的关系正确的是( )
①物质的量之比为1:2 ②物质的量之比是3:1
③质量之比是2:1 ④质量之比是4:1.
①物质的量之比为1:2 ②物质的量之比是3:1
③质量之比是2:1 ④质量之比是4:1.
| A、②④ | B、②③ | C、①④ | D、只有④ |
2001年诺贝尔化学奖授予在“手性碳原子的催化氢化、氧化反应”研究领域作出贡献的美、日三位科学家.下列分子含有手性碳原子的是( )
| A、CHFBr2 |
| B、CH3CH2OH |
C、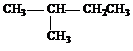 |
D、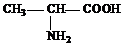 |
下列离子方程式书写正确的是( )
| A、硫酸亚铁的酸性溶液中加过氧化氢溶液:Fe2++H2O2+2H+═Fe3++2H2O |
| B、NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32- |
| C、NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O |
| D、Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
用NA表示阿伏加德常数,下列叙述中正确的是( )
A、在标准状况下,1L庚烷完全燃烧后,所生成的气态产物的分子数为
| ||
| B、1mol碳正离子CH5+所含的电子数为10NA | ||
| C、标准状况下,16g甲烷完全燃烧所消耗的氧气的分子数的3NA | ||
| D、0.5molC3H8分子中含C-H共价键2NA |
交警执法查处酒驾时,主要测量驾驶员体内的( )
| A、醋酸 | B、乙醇 | C、甲醛 | D、葡萄糖 |
不能通过化合反应直接得到的化合物是( )
| A、FeCl2 |
| B、Na2S |
| C、Fe(OH)3 |
| D、Al(OH)3 |