物质在反应中可表现氧化性、还原性、酸性、碱性等,下面反应的划线物质中,能在同一反应中同时表现上述两种或两种以上性质的有( )
①3FeO+10HNO3═3Fe(NO3)3+NO↑+5H2O
②C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O
③8NH3+3Cl2═6NH4Cl+N2
④NaH+H2O═NaOH+H2↑
⑤2Na2O2+2H2O═4NaOH+O2↑
①3FeO+10HNO3═3Fe(NO3)3+NO↑+5H2O
②C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O
③8NH3+3Cl2═6NH4Cl+N2
④NaH+H2O═NaOH+H2↑
⑤2Na2O2+2H2O═4NaOH+O2↑
| A、仅有①② | B、仅有①③④⑤ |
| C、仅有①③⑤ | D、全部 |
下列叙述正确的是( )
A、因为Na2CO3+SiO2
| ||||
| B、碳和硅都是ⅣA族的元素,所以二氧化碳和二氧化硅的物理性质相似 | ||||
| C、二氧化硅既溶于氢氧化钠溶液又溶于氢氟酸,所以二氧化硅是两性氧化物 | ||||
| D、二氧化硅和二氧化碳都是酸性氧化物,但二氧化硅不能和水反应生成硅酸 |
下列事实不能用勒夏特列原理解释的是( )
| A、黄绿色的氯水光照后颜色变浅 |
| B、在SO2氧化为SO3的过程中使用催化剂 |
| C、由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅 |
| D、在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去 |
下列化工生产过程不是氧化还原反应的是( )
| A、氮气与氢气合成氨 |
| B、氨气为原料制硝酸 |
| C、磷矿石跟硫酸制磷肥 |
| D、铁矿石炼制生铁 |
设NA为阿伏加德罗常数的值,下列判断正确的是( )
| A、1 mol/LAlCl3溶液,含有Al3+的数目为NA |
| B、标准状况下,22.4LCCl4中分子数目为NA |
| C、0.1mol Fe与过量的稀硫酸充分反应,转移的电子数为0.3 NA |
| D、O2和O3组成的48g混合气体中含有3 NA个氧原子 |
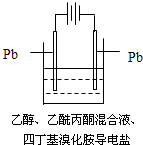 有机电解制备的金属醇盐,可直接作为制备纳米材料的前体.以下是一种电化学合成金属醇盐的主要装置.在电解过程中,已知乙醇和乙酰丙酮(CH3COCH2COCH3)在阴极发生的电极反应为:
有机电解制备的金属醇盐,可直接作为制备纳米材料的前体.以下是一种电化学合成金属醇盐的主要装置.在电解过程中,已知乙醇和乙酰丙酮(CH3COCH2COCH3)在阴极发生的电极反应为:2CH3CH2OH+2e-=2CH3CH2O-+H2↑
2CH3COCH2COCH3+2e-=2(CH3COCHCOCH3)+H2↑
下列说法正确的是( )
| A、阳极Pb失去电子,发生还原反应 |
| B、当阳极失去2 mol e-时,阴极产生2 mol氢气 |
| C、电解过程中,阳离子向阴极移动 |
| D、已知Pb-4e-=Pb4+,当消耗Pb的质量为103.5 g时,则转移电子2 mol |
水溶液中能大量共存的一组离子是( )
| A、Al3+、Na+、CO32-、NO3- |
| B、Ag+、Cl-、Fe3+、HCO3- |
| C、Fe2+、H+、K+、MnO4- |
| D、Mg2+、Br-、NH4+、SO42- |
有关说法正确的是( )
| A、0.1mol/L NH4C1溶液加蒸馏水稀释,溶液的pH不断减小 |
| B、常温下,pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7 |
| C、NH4HSO4溶液中滴加NaOH溶液至溶液pH=7,则c(Na+)=2c(SO42-) |
| D、0.1mol/L的NaHA溶液,其pH=4时:c(HA-)>c(H+)>c(H2A)>c(A2-) |
下列粒子在溶液中能大量共存的一组是( )
A、Ca2+、Na+、HCO
| ||||
| B、Al3+、K+、CO32-、Cl- | ||||
C、Fe3+、Cu2+、SCN-、SO
| ||||
D、Fe2+、H+、SO
|
在一定温度下,某浓度的HNO3与Zn反应,生成NO2和NO的物质的量之比为1:3,则要使1mol Zn完全反应,需要HNO3的物质的量为( )
| A、2.8mol |
| B、2.6mol |
| C、2.4mol |
| D、0.8mol |