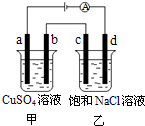
 如图,a、b、c、d均为石墨电极,通电进行电解.下列说法正确的是( )
如图,a、b、c、d均为石墨电极,通电进行电解.下列说法正确的是( )| A、乙烧杯中d的电极反应为 2Cl--2e-═Cl2↑ |
| B、a、c两极产生气体的物质的量相等 |
| C、甲、乙两烧杯中溶液的pH均保持不变 |
| D、乙烧杯中通入适量HCl气体,溶液组成可以恢复 |
采用下列装置和操作,能达到实验目的是( )
A、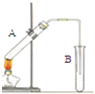 A中为乙醇、醋酸,B中为饱和碳酸钠溶液,制取乙酸乙酯 |
B、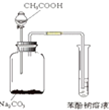 验证醋酸、碳酸、苯酚的酸性强弱 |
C、 用浓硫酸、乙醇共热到约170℃制乙烯 |
D、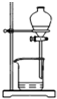 用NaOH溶液除去苯中混有的少量苯酚 |
有机物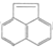 的一元取代产物有( )
的一元取代产物有( )
 的一元取代产物有( )
的一元取代产物有( )| A、8神 | B、6种 | C、4种 | D、3种 |
实验室进行下列有关物质的准备,理论上正确、操作上可行、经济上合理的是( )
A、C
| ||||||
B、Cu
| ||||||
C、CaO
| ||||||
D、Fe
|
短周期元素甲、乙、丙、丁的原子序数依次增大,甲是周期表中原子半径最小的元素,乙的单质在暗处与甲的单质剧热反应化合并发生爆炸,甲和丙同主族,丁的最外层电子数和电子层数相等,则( )
| A、原子半径:丙>丁>乙 |
| B、甲与丙的原子核外电子数相差8 |
| C、丙的单质在空气中燃烧生成只含离子键的化合物 |
| D、最高价氧化物对应的水化物的碱性:丙>丁 |
最近,美国普度大学的研究人员开发出一种利用铝镓合金加水制造氢气的新工艺.这项技术具有广泛的能源潜在用途,包括为汽车提供原料、潜水艇提供燃料等.该技术通过向铝镓合金注水,铝生成氧化铝,同时生成氢气.合金中镓(Ga)是关键成分,可阻止铝形成致密的氧化膜.下列关于铝、镓的说法正确的是( )
| A、铝、镓合金与水反应后的物质可以回收利用冶炼铝 |
| B、铝的金属性比镓强 |
| C、铝镓合金的熔点比铝低 |
| D、Ga(OH)3与Al(OH)3性质相似,能与NaOH溶液反应 |
下列离子方程式正确的是( )
A、等体积、等物质的量浓度的Ca(HCO3)2溶液和NaOH溶液混合:Ca2++2HCO
| ||||
| B、向明矾溶液中滴加氢氧化钡溶液至SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O | ||||
| C、1molCl2通入含1mol FeI2的溶液中:2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2 | ||||
| D、酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O=3I2+6OH- |
在1L定容的密闭容器中,可以证明可逆反应N2+3H2? 2NH3 已达到平衡状态的是( )
| A、c(N2):c(H2):c(NH3)=1:3:2 |
| B、一个N≡N 断裂的同时,有3个H-H生成 |
| C、其他条件不变时,混合气体的密度不再改变 |
| D、v正(N2)═2 v逆(NH3) |
下列说法错误的是( )
| A、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| B、利用丁达尔效应可以区别溶液与胶体 |
| C、质子数相同的粒子不一定是同一种元素 |
| D、1 mol CH4燃烧所放出的热量是CH4的燃烧热 |