下列离子方程式书写正确的是( )
| A、过量氯气通入溴化亚铁溶液中:3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2 |
| B、FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+ |
| C、NO2与水的反应:3NO2+H2O=2NO3-+NO+2H+ |
| D、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O |
下列说法正确的是( )
| A、F、Cl、Br的最外层电子数都是7,次外层电子数都是8 |
| B、从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增规律 |
| C、卤素按F、Cl、Br、I的顺序其非金属性逐渐减弱的原因是随着核电荷数增加电子层数增大起主要作用 |
| D、砹是原子序数最大的卤族元素,根据卤素性质的递变规律,砹易溶于水,难溶于CCl4 |
下列反应中,水作为还原剂的是( )
| A、2F2+2H2O═4HF+O2 |
| B、NaOH+HCl═NaCl+H2O |
| C、2Na+2H2O═2Na++2OH-+H2↑ |
| D、Cl2+H2O═HCl+HClO |
阿伏加德罗常数为NA,下列说法中正确的是( )
| A、1.0L 1.0 mol?L-1NaNO3溶液中含有的氧原子数为3NA |
| B、在标准状况下,22.4LCO2和O2混合气体中含有的氧原子数为NA |
C、 31 g P4 (分子结构如图)中含有的P-P键个数为1.5NA 31 g P4 (分子结构如图)中含有的P-P键个数为1.5NA |
| D、0.1mol Fe在0.1mol C12中充分燃烧,转移的电子数为0.3NA |
下列事实一般不能用于判断金属性强弱的是( )
| A、金属的颜色和熔沸点 |
| B、金属元素的最高价氧化物对应的水化物的碱性强弱 |
| C、1mo金属单质在反应中失去电子的多少 |
| D、金属元素的单质和水或酸置换出氢的难易 |
某学习小组辨析以下说法:
①纳米材料和蛋白质溶液都有丁达尔效应;
②天然气和沼气的主要成分都是甲烷;
③棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2O;
④制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料;
⑤冰水混合物和干冰既是纯净物又是化合物;
⑥粗盐和酸雨都是混合物;
⑦金属材料都是导体,非金属材料都是绝缘体.
正确的是( )
①纳米材料和蛋白质溶液都有丁达尔效应;
②天然气和沼气的主要成分都是甲烷;
③棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2O;
④制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料;
⑤冰水混合物和干冰既是纯净物又是化合物;
⑥粗盐和酸雨都是混合物;
⑦金属材料都是导体,非金属材料都是绝缘体.
正确的是( )
| A、①②④ | B、②⑤⑥ |
| C、③⑤⑦ | D、②⑥⑦ |
分子式为C4H8O2的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,这些醇和酸重新组合可形成的酯共有( )
| A、1种 | B、5种 | C、9种 | D、12种 |
某有机化合物的结构简式如图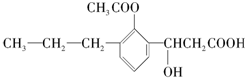 此有机化合物属于( )
此有机化合物属于( )
①烯烃 ②多官能团有机化合物 ③芳香烃 ④烃的衍生物 ⑤高分子化合物 ⑥酚类.
 此有机化合物属于( )
此有机化合物属于( )①烯烃 ②多官能团有机化合物 ③芳香烃 ④烃的衍生物 ⑤高分子化合物 ⑥酚类.
| A、①②③④ | B、②④ |
| C、②④⑤ | D、①③⑤⑥ |
化学平衡状态是( )
| A、静止止状态 |
| B、正反应速率大于逆反应速率 |
| C、不可改变的状态 |
| D、反应物与生成物浓度保持不变的状态 |
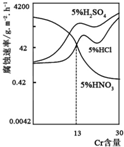 如图是三种酸对Fe-Cr合金随Cr含量变化的腐蚀性实验结果,下列有关说法正确的是( )
如图是三种酸对Fe-Cr合金随Cr含量变化的腐蚀性实验结果,下列有关说法正确的是( )| A、稀硫酸对Fe-Cr合金的腐蚀性比稀硝酸和稀盐酸都强 |
| B、随着Fe含量的增加,Fe-Cr合金在5%HNO3中的耐腐蚀性越来越弱 |
| C、Cr含量等于13%时,三种酸对Fe-Cr合金的腐蚀速率由快到慢的顺序为H2SO4>HCl>HNO3 |
| D、Cr含量小于13%时,因为三种酸中硫酸的氢离子浓度最大,所以对Fe-Cr合金的腐蚀性最强 |