M元素的一个原子失去两个电子并转移到Y元素的两个原子中,形成离子化合物Z,下列说法不正确的是( )
| A、Z的熔点较高 |
| B、Z可以表示为M2Y |
| C、Z一定溶于水 |
| D、M形成+2价的阳离子 |
设NA为阿伏加德罗常数的值.下列说法中正确的是( )
| A、在密闭容器中加入1 mol N2和3 mol H2,充分反应生成NH3分子数为2NA |
| B、标准状况下,4.48 L N2所含的共用电子对数0.2NA |
| C、常温常压下,1 mol NaHSO4晶体中含有2NA个离子 |
| D、标准状况下,1 mol Fe与2.24 L Cl2反应转移的电子数为3NA |
A元素的阳离子与B元素的阴离子具有相同的电子层结构,有关两元素有以下叙述:①原子半径A<B ②离子半径A>B ③原子序数A>B ④原子最外层电子数A=B⑤A的正价与B的负价绝对值不一定相等.其中一定正确的是( )
| A、①② | B、③④⑤ | C、③⑤ | D、③④ |
用NA表示阿伏加德罗常数的值,下列说法不正确的是( )
| A、常温下,1 L0.1mol/LNa2CO3溶液中,含有阴离子的总数小于0.1 NA |
| B、常温常压下,Na2O2与足量H2O反应,共生成0.2mol O2,转移电子的数目为0.4NA |
| C、5.6 g铁和6.4 g铜分别与0.1 mol氯气完全反应,转移的电子数相等 |
| D、84 gNaHCO3与MgCO3的混合物中所含氧原子数目一定为3NA |
电子数相同的两种粒子我们称二者为等电子体.如Na+和NH4+均为10电子粒子.下列物质中,不属于C3O2的等电子体的是( )
| A、N5+ |
| B、C2NO2+ |
| C、NCN2O |
| D、NC3O- |
设NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、0.1 mol H2O和D2O组成的混合物中含有的中子数是NA |
| B、常温常压下,NO2和N2O4的混合物46g中约含有2NA个氧原子 |
| C、1 mol CH3+(碳正离子)中含有电子数为10NA |
| D、在Cu-Zn原电池中,正极产生1.12LH2时,负极产生了0.05 NA 个 Zn2+ |
某混合物A中,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化.据此判断:
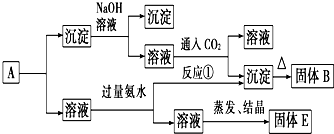
(1)操作a的名称为
(2)固体B所含物质的化学式
(3)反应①的离子反应方程为 .

(1)操作a的名称为
(2)固体B所含物质的化学式
(3)反应①的离子反应方程为
 设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )