在Al2(SO4)3、K2SO4和KAl(SO4)2的混合溶液中,如果SO42-的物质的量浓度为0.2mol?L-1,当加等体积的0.2mol?L-1的KOH溶液时,生成的沉淀恰好溶解,则原混合物中K+的物质的量浓度是( )
| A、0.2 mol?L-1 |
| B、0.25 mol?L-1 |
| C、0.45 mol?L-1 |
| D、0.225 mol?L-1 |
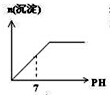
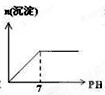
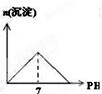
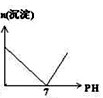
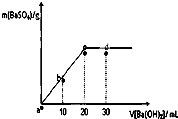 常温下,向0.25mol?L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中不正确的是( )
常温下,向0.25mol?L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中不正确的是( )| A、硫酸溶液的体积为20 mL |
| B、b时刻溶液中硫酸根离子浓度约为0.125 mol?L-1 |
| C、d时刻溶液的pH为13 |
| D、溶液的导电能力:c<d<b<a |
 某同学在研究前18号元素时发现,可以将它们排成如图所示的蜗牛形状,图中每个点代表-种元素,其中0点代表氢元素.下列说法中正确的是( )
某同学在研究前18号元素时发现,可以将它们排成如图所示的蜗牛形状,图中每个点代表-种元素,其中0点代表氢元素.下列说法中正确的是( )| A、虚线相连的元素处于同一族 |
| B、离0点越远的元素原子半径越大 |
| C、.B、C最高价氧化物的水化物可相互反应 |
| D、A、B组成的化合物中不可能含有共价键 |
下列分子中所有原子都满足最外层为8电子结构的是( )
| A、SiCl4 |
| B、H2O |
| C、BF3 |
| D、PCl5 |
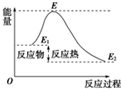
下列说法不正确的是( )

| A、反应物分子(或离子)间的每次碰撞是反应的先决条件 |
| B、反应物的分子的每次碰撞都能发生化学反应 |
| C、活化分子具有比普通分子更高的能量,催化剂能够减低活化能的数值 |
| D、活化能是活化分子的平均能量与所有分子平均能量之差,如图所示正反应的活化能为E-E1 |
下列与化学反应能量变化相关的叙述正确的是( )
| A、生成物总能量一定低于反应物总能量 |
| B、等量H2在O2中完全燃烧,生成H2O(g)与生成H2O(l)放出的能量相同 |
| C、应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
有4种燃料电池下面是工作原理示意图,其中正极反应的产物为水的是( )
A、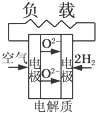 固体氧化物燃料电池 |
B、 碱性氢氧燃料电池 |
C、 质子交换膜燃料电池 |
D、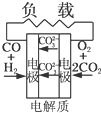 熔融盐燃料电池 |
科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰.电池总反应为:Zn+2MnO2+H2O═ZnO+2MnO(OH).下列说法正确的是( )
| A、该电池反应中MnO2起催化作用 |
| B、该电池的正极反应为:MnO2-e-+H2O═MnO(OH)+OH- |
| C、导电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn |
| D、电池工作时,负极周围溶液的pH将不断变大 |
 元素周期表中,金属和非金属分界线附近的元素性质特殊.其单质和化合物应用广
元素周期表中,金属和非金属分界线附近的元素性质特殊.其单质和化合物应用广