对于可逆反应mA(g)+nB(s)?pC(g)+qD(g)反应过程中,其他条件不变时,产物D的质量分数D%与温度T或压强p?的关系如图所示,请判断下列说法正确的是( )
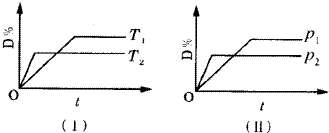

| A、降温,化学平衡向逆反应方向移动 |
| B、使用催化剂可使D%有所增加 |
| C、化学方程式中气体的化学计量数m<p+q? |
| D、B的颗粒越小,正反应速率越快,有利于平衡向正反应方向移动 |
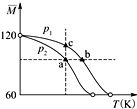 已知(CH3COOH)2(g)?2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量随温度(T)的变化曲线如图所示,下列说法正确的是( )
已知(CH3COOH)2(g)?2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量随温度(T)的变化曲线如图所示,下列说法正确的是( )| A、该过程的△H<0 |
| B、气体压强:p(a)<p(b)=p(c) |
| C、平衡常数:K(a)=K(b)<K(c) |
| D、测定乙酸的相对分子质量要在高压、低温条件 |
某化学科研小组研究合成氨:N2(g)+3H2(g)═2NH3(g);△H<0,在其他条件不变时,改变某一条件时对化学平衡的影响,得到如下图象,以下对应选项中正确的是( )
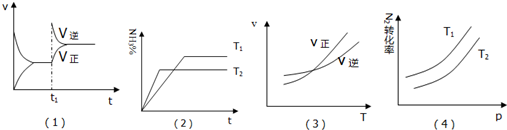

| A、(1)对应的是:在t1时恒压条件下,通入NH3 |
| B、(2)对应的是:氨气在恒容不同温度下的百分含量 |
| C、(3)对应的是:在恒容条件下,反应速率与温度的关系 |
| D、(4)对应的是:N2转化率与温度(T1>T2)、压强的关系 |
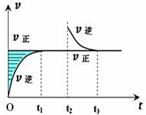 某恒温密闭容器发生可逆反应M (?)+N(?)═Q(g)+P(?)△H,如图所示,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列说法中正确的是( )
某恒温密闭容器发生可逆反应M (?)+N(?)═Q(g)+P(?)△H,如图所示,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列说法中正确的是( )| A、M和N在该条件下至少有一种是气态 |
| B、t2时刻后该可逆反应向逆反应方向进行,P的浓度一定减小 |
| C、若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大 |
| D、若在该温度下此反应平衡常数表达式为K=c(Q),则t1~t2时间段与t3时刻后的Q浓度不相等 |
下列混合溶液中,各离子浓度的大小顺序正确的是( )
| A、10 mL 0.1 mol/L氨水与10 mL 0.1 mol/L盐酸混合,c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B、10 mL 0.1 mol/L NH4Cl溶液与5 mL 0.2 mol/L NaOH溶液混合,c(Na+)=c(Cl-)>c(OH-)>c(H+) |
| C、10 mL 0.1 mol/L CH3COOH溶液与5 mL 0.2 mol/L NaOH溶液混合,c(Na+)=c(CH3COO-)>c(OH-)>c(H+) |
| D、10 mL 0.5 mol/L CH3COONa溶液与6 mL 1 mol/L盐酸混合,c(Cl-)>c(Na+)>c(OH-)>c(H+) |
下列溶液中,微粒浓度关系正确的是( )
| A、常温下,pH=6的由醋酸与醋酸钠组成的混合溶液中:c(Na+)>c(CH3COO-) |
| B、将Cl2通入过量KOH溶液中:c(ClO-)+c(Cl-)=c(K+) |
| C、0.1mol?L-1的Na2S溶液中:c(OH-)=c(H+)+c(HS-)+2c(H2S) |
| D、室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
 有两只密闭容器A和B,A能保持恒压,B能保持恒容.起始时向容积相等的A、B中分别通入体积比为2:1的等量的SO2和O2,使之发生反应:2SO2+O2?2SO3,并达到平衡.则(填>、=、<;左、右;增大、减小、不变).
有两只密闭容器A和B,A能保持恒压,B能保持恒容.起始时向容积相等的A、B中分别通入体积比为2:1的等量的SO2和O2,使之发生反应:2SO2+O2?2SO3,并达到平衡.则(填>、=、<;左、右;增大、减小、不变).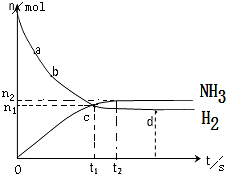 合成氨工业对国民经济和社会发展具有重要的意义.一定温度下,在2L的密闭容器中加入一定量的N2和H2,发生合成氨反应,其中n(NH3)和n(H2)随时间变化的关系如图所示.
合成氨工业对国民经济和社会发展具有重要的意义.一定温度下,在2L的密闭容器中加入一定量的N2和H2,发生合成氨反应,其中n(NH3)和n(H2)随时间变化的关系如图所示.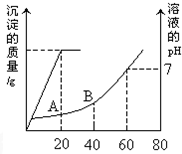 (1)某温度下,纯水中的c(H+)=2.0×10-7mol/L,此时溶液的c(OH-)=
(1)某温度下,纯水中的c(H+)=2.0×10-7mol/L,此时溶液的c(OH-)=