奥运会上发令枪所用“火药”的主要成分是氯酸钾和红磷,撞击时发生化学反应:5KClO3+6P=3P2O5十5KCl.而我国古代“火药”的成分是木炭粉(C)、硫磺(S)、硝石(KNO3),经点燃发生的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑,则下列有关叙述中错误的是( )
| A、两个反应中还原产物前者为KCl,后者为K2S和N2 |
| B、两个反应均为置换反应 |
| C、若两个反应中生成等物质的量的P2O5和CO2转移电子数之比为5:2 |
| D、火药中的钾盐均作氧化剂 |
被称为万能还原剂的NaBH4溶于水并和水反应:NaBH4+2H2O═NaBO2+4H2↑.下列说法中正确的是( )
| A、被氧化的元素与被还原的元素质量比为1:4 |
| B、NaBH4既是氧化剂又是还原剂 |
| C、NaBH4是还原剂,H2O是氧化剂 |
| D、硼元素被氧化,氢元素被还原 |
298K时,合成氨反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.在该温度下取2mol N2和6mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量( )
| A、等于92.4 kJ |
| B、等于184.8 kJ |
| C、小于184.8 kJ |
| D、大于184.8 kJ |
取0.2mol/L HX溶液与0.2mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8(25°C),则混合溶液中下列说法(或关系式)不正确的是( )
| A、由水电离出的c(OH-)=1×10-6 mol/L |
| B、c(Na+)=c(X-)+c(HX) |
| C、c(Na+)-c(OH-)=c(X-)-c(H+) |
| D、c(X-)=c(Na+)>c(OH-)=c(H+) |
中和相同体积、相同pH的Ba(OH)2、NaOH、NH3?H2O三种溶液,所用相同浓度的盐酸的体积分别是V1、V2、V3,则三者的关系是( )
| A、V1=V2=V3 |
| B、V1>V2>V3 |
| C、V3>V1>V2 |
| D、V1=V2<V3 |
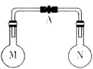 室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是( )| 编号 | ① | ② | ③ | ④ |
| 气体M | H2S | H2 | NH3 | NO |
| 气体N | SO2 | Cl2 | HCl | O2 |
| A、①②③④ | B、①④③② |
| C、②④①③ | D、④①②③ |
下列事实的解释正确的是( )
| A、将SO2、SO3 混合气体通入氯化钡溶液中,出现浑浊是因为生成了BaSO4沉淀 | ||||
| B、SO2通入溴水中,溴水褪色,是因为SO2的漂白性 | ||||
C、反应2C+SiO2
| ||||
| D、在NaHCO3的溶液中滴加NaAlO2溶液中有白色沉淀生成,是因为二者发生完全水解反应 |
常温下,等体积的下列各组酸和碱的溶液混和后,溶液pH<7的是( )
①pH之和为14的硝酸和氢氧化钾溶液;
②pH之和为15的盐酸和氨水溶液;
③pH之和为14的醋酸和苛性钠溶液;
④pH之和为13的硫酸和氢氧化钡溶液.
①pH之和为14的硝酸和氢氧化钾溶液;
②pH之和为15的盐酸和氨水溶液;
③pH之和为14的醋酸和苛性钠溶液;
④pH之和为13的硫酸和氢氧化钡溶液.
| A、② | B、①② | C、②③ | D、③④ |
常温下,下列关于酸碱反应的说法正确的是( )
| A、用pH=2和pH=3的醋酸溶液中和含等量NaOH的溶液所消耗醋酸溶液体积分别为Va,Vb,则Vb<10Va |
| B、pH=2的HCl与pH=12的NH3?H2O 等体积混合后溶液是酸性 |
| C、向体积为V1L的浓度均为0.1mol/L HCl、CH3COOH混合溶液中加入 V2L 0.2mol/L的NaOH溶液后,溶液呈中性,则V1>V2 |
| D、pH为2的硫酸与0.01mol/L的NaOH溶液等体积混合后,混合溶液显酸性 |