下列有关微粒或物质的“量”的叙述不正确的是( )
| A、浓度分别为2mol/L和1mol/L的Na2CO3溶液中,C(CO32-)的比值为2:1 |
| B、常温常压下,16g 02和O3混合气体中含有NA个氧原子 |
| C、46gNO2和N204混合气体的物质的量之和大于O.5mol,小于lmol |
| D、向饱和CuS04溶液中加入1 mol CuS04固体,则析出的晶体的质量大于250g |
下列现象或应用中,与胶体有关,且说法正确的是( )
| A、清晨,在茂密的树木中,常常可以看到从枝叶间透过的道道光柱 |
| B、在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色的Fe(OH)3胶体 |
| C、向有污染的水中加入胶体,具有杀菌消毒的作用 |
| D、将Fe(OH)3胶体放置一段时间后,会出现浑浊 |
下列有关Fe2(SO4)3,溶液的叙述正确的是( )
| A、和KI溶液反应的离子方程式:Fe3++2I-═Fe2++I2 |
| B、硫酸铁和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ |
| C、1L0.1mol/L该溶液和足量的Zn充分反应,生成11.2gFe |
| D、该溶液中,K+、Fe3+、C6H5OH、Br-可以大量共存 |
下列有关化学用语表示正确的是( )
A、对硝基甲苯的结构简式: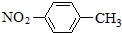 | ||
B、氯化铵的电子式: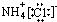 | ||
C、中子数为16的硫原子:
| ||
| D、乙炔的最简式:CH |
纳米材料是指颗粒的三维线度中的任一维在1nm~100nm范围的材料.纳米技术所带动的技术革命及其对人类的影响,远远超过电子技术.下列关于纳米技术的叙述不正确的是( )
| A、将纳米材料分散到液体分散剂中可制得液溶胶 |
| B、用纳米级金属颗粒粉剂作为催化剂可加快化学反应速率 |
| C、将单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧,说明“纳米铜”比铜片更易失电子 |
| D、银器能抑菌、杀菌,将纳米银粒子植入内衣织物中,有奇异的抑菌、杀菌效果 |
下列现象或性质与胶体无关的是( )
| A、日常生活中看到的烟、云、雾 |
| B、明矾可做净水剂 |
| C、向FeCl3溶液中滴加烧碱溶液,得到红褐色浑浊的分散系 |
| D、向沸水中逐滴加入FeCl3饱和溶液,得到红褐色透明的分散系 |
下列离子方程式书写正确的是( )
| A、碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32++2H2O |
| B、用氨水吸收过量的二氧化硫 NH3?H2O+SO2=NH4++HSO3- |
| C、次氯酸钙溶液中通人过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO |
| D、氯化亚铁溶液中加入硝酸:2Fe2++4H++NO3-=2Fe3++2H2O+NO↑ |
以下化学反应不属于氧化还原反应的是( )
| A、2Na+2H2O═2NaOH+H2↑ |
| B、N2H4+O2═N2+2H2O |
| C、FeO+2HCl═FeCl2+H2O |
| D、NO+NO2+Na2CO3═2NaNO2+CO2↑ |
下列反应的离子方程式正确的是( )
| A、NaAlO2溶液中通入过量的CO2:2AlO2-+3H2O+CO2═2Al(OH)3↓+CO32- |
| B、明矾溶液中滴加Ba(OH)2溶液至SO42-完全沉淀:Al3++Ba2++SO42-+3OH-═BaSO4↓+Al(OH)3↓ |
| C、200 mL 2 mol/L的FeBr2溶液中通入11.2 L标准状况下的氯气:4Fe2++6Br-+5Cl2═4Fe3++3Br2+10Cl- |
| D、在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
三氟化氮(NF3)是微电子工业中一种优良的等离子蚀刻气体,无色.无臭,在潮湿空气中泄露会产生白雾.红棕色气体等现象,反应方程式为:aNF3+bH2O=c +dHNO3+eHF.下列说法正确的是( )
| A、反应方程式横线处物质为NO,且a=3,b=5,c=2,d=1,e=9 |
| B、反应中被氧化与被还原的原子物质的量之比为2:1 |
| C、若反应中生成0.2molHNO3,则反应共转移0.2mole- |
| D、反应中NF3是氧化剂,H2O是还原剂 |