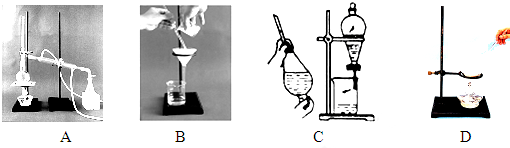
下列实验操作中,主要不是从安全因素考虑的是( )
| A、点燃氢气前一定要检验氢气的纯度 |
| B、未使用完的白磷要随时收集起来,并与空气隔绝 |
| C、用氢气还原氧化铜时,要先通一会儿氢气,再加热氧化铜 |
| D、酒精灯不用时,必须盖上灯帽 |
下列有关化学实验的叙述正确的是( )
| A、用待测液润洗滴定用的锥形瓶 |
| B、滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定 |
| C、玻璃棒蘸取溶液滴到放在表面皿上的pH试纸上 |
| D、Na2CO3溶液保存在带玻璃塞的试剂瓶中 |
下列说法正确的是( )
| A、已知a g乙烯气体充分燃烧时生成1 mol CO2和液态水,放出b kJ的热量,则表示乙烯燃烧热的热化学方程式为2C2H4(g)+6O2(g)═4CO2(g)+4H2O(l)△H=-4b kJ?mol-1 | ||||
| B、已知:H2(g)+F2(g)═2HF(g)△H=-270 kJ?mol-1,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ | ||||
C、500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)
| ||||
| D、已知:①C(s,石墨)+O2(g)═CO2(g)△H=-393.5 kJ?mol-1,②C(s,金刚石)+O2(g)═CO2(g)△H=-395.0 kJ?mol-1,则C(s,金刚石)═C(s,石墨)△H=-1.5 kJ?mol-1 |
pH值测定是检验物质的常用方法,下列有关pH值测定的实验合理的是( )
| A、将失去标签的Na2CO3和NaHCO3固体样品配成等物质的量浓度溶液,分别测定pH值,以此鉴别这两种固体 |
| B、用pH试纸分别测定氯水和盐酸的pH值,比较两溶液的酸性强弱 |
| C、取同体积不同浓度的醋酸和盐酸加水稀释相同倍数,测定稀释前后pH值的变化,以此区别这两种酸 |
| D、测定硫酸型酸雨的pH值时,取样后应立即测定 |
对热化学方程式C(s)+H2O(g)═CO(g)+H2(g)△H=+131.3kJ?mol-1最准确的理解是( )
| A、碳和水反应吸收131.3 kJ热量 |
| B、1 mol碳和1 mol水反应生成一氧化碳和氢气,同时放出131.3 kJ热量 |
| C、1 mol碳和1 mol水蒸气反应生成1 mol CO和1 mol H2,同时吸收131.3 kJ热量 |
| D、1个固态碳原子和1分子水蒸气反应吸热131.1 kJ |
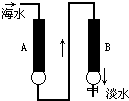 钠型离子交换剂磺化煤(NaR)可使硬水的Ca2+、Mg2+通过离子交换而软化.现代海水的淡化方法是使海水(含Na+、Mg2+、Ca2+、Cl-等)依次通过两种离子交换树脂A、B(如图所示),下列说法不正确的是( )
钠型离子交换剂磺化煤(NaR)可使硬水的Ca2+、Mg2+通过离子交换而软化.现代海水的淡化方法是使海水(含Na+、Mg2+、Ca2+、Cl-等)依次通过两种离子交换树脂A、B(如图所示),下列说法不正确的是( )| A、A为氢型阳离子交换树脂(HR),B为羟型阴离子换树脂(ROH) |
| B、A为羟型阳离子交换树脂(ROH),B为氢型阳离子交换树脂(HR) |
| C、HR与Na+的反应可表示为HR+Na+═NaR+H+ |
| D、由中性海水用此方法得到的淡水pH不变 |
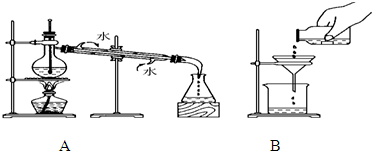
下列混合物能用分液法分离的是( )
| A、乙醇与乙酸 |
| B、苯和溴苯 |
| C、乙酸乙酯和Na2CO3溶液 |
| D、葡萄糖与水的混合液 |
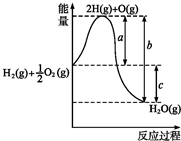 (1)已知:H2(g)+O2(g)═H2O(g),反应过程中能量变化如图所示,则:
(1)已知:H2(g)+O2(g)═H2O(g),反应过程中能量变化如图所示,则: