研究表明,化学反应中的能量变化其本质是化学键的生成或断裂过程中分别会释放与吸收能量.如图表示反应2H2(g)+O2(g)═2H2O(g)的能量变化,下列有关说法中错误的是( )


| A、图中的①是指吸收能量,②是指放出能量 |
| B、图示说明反应2H2(g)+O2(g)═2H2O(g)是一个吸热反应 |
| C、图示说明化学键的形成与断裂是物质在化学反应中发生能量变化的主要原因 |
| D、③中a所指的数值为484 |
 可逆反应mA(g)+nB(g)?pC(g)+gD(g)的v-t图象如图Ⅰ所示,若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图象如图Ⅱ所示.
可逆反应mA(g)+nB(g)?pC(g)+gD(g)的v-t图象如图Ⅰ所示,若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图象如图Ⅱ所示. ①a1=a2
②a1<a2
③b1=b2
④b1<b2
⑤t1>t2 ⑥t1=t2
⑦两图中阴影部分面积相等
⑧图Ⅱ中阴影部分面积更大
以上所列正确的为( )
| A、②④⑤⑦ | B、②④⑤⑧ |
| C、②③⑤⑦ | D、②③⑤⑧ |
 有一反应,由X与Y化合生成Z.其反应如右:2X+3Y=2Z,反应物X与生成物Z的质量关系如图.下列说法正确的是( )
有一反应,由X与Y化合生成Z.其反应如右:2X+3Y=2Z,反应物X与生成物Z的质量关系如图.下列说法正确的是( )| A、有4g的Z生成时,则消耗Y 6g |
| B、X、Y、Z的摩尔质量之比为3:2:6 |
| C、2mol X质量与3mol Y质量之和等于2mol Z的质量 |
| D、消耗2mol X时,在标准状况下,生成Z的体积为44.8L |
1.52g 铜镁合金完全溶解于50mL 密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
| A、该合金中铜与镁的物质的量之比是2:1 |
| B、得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL |
| C、NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D、该浓硝酸中HNO3的物质的量浓度是14.0 mol/L |
在一定条件下,NO能跟H2发生如下反应:2NO+2H2═N2+2H2O.经研究,上述反应是按以下三步反应依次进行的总反应(括号中是该条件下反应的相对速率):(Ⅰ)2NO+H2═N2O+H2O(慢);(Ⅱ)2N2O═2N2+O2(快);(Ⅲ)2H2+O2═2H2O(更快).以上总反应的速率主要取决于三步反应中的( )
| A、(Ⅰ) | B、(Ⅱ) |
| C、(Ⅲ) | D、(Ⅱ)和(Ⅲ) |
W克下列物质电火花引燃后的产物通过足量的Na2O2后,固体增重大于W克的是( )
| A、CO与H2的混合气体 |
| B、CH3CH2OH |
| C、HCOOH |
| D、CH3COOH |
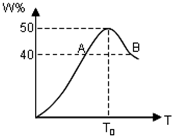 2L容器中,分别将物质的量均为2.00mol的X、Y混合,在不同温度(T)下发生如下反应:2X(g)+Y(g)?2W(g).并在第10s时分别测定其中W的体积分数(W%),并绘成如图所示曲线:
2L容器中,分别将物质的量均为2.00mol的X、Y混合,在不同温度(T)下发生如下反应:2X(g)+Y(g)?2W(g).并在第10s时分别测定其中W的体积分数(W%),并绘成如图所示曲线:
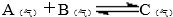 )前起始体积相同、且容积固定的容器中发生上述反应开始时放入1mol A和1mol B到达平衡后生成bmol C.将b与(1)小题中的a进行比较
)前起始体积相同、且容积固定的容器中发生上述反应开始时放入1mol A和1mol B到达平衡后生成bmol C.将b与(1)小题中的a进行比较