某温度下,在一个2L的密闭容器中加入4mol A和2mol B进行如下反应:3A(g)+2B(g)?4C(s)+D(g),反应2min后达到平衡,测得生成1.6mol C,下列说法正确的是( )
| A、前2 min D的平均反应速率为0.2 mol?L-1?min-1 |
| B、此时,B的平衡转化率是40% |
| C、增大该体系的压强,平衡不移动 |
| D、增加B,平衡向右移动,B的平衡转化率增大 |
把3mol A和2.5mol B混合于2L密闭容器中,发生反应:
3A(g)+B(g)?xC(g)+2D(g),5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L?min),下列结论正确的是( )
3A(g)+B(g)?xC(g)+2D(g),5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L?min),下列结论正确的是( )
| A、平衡时,B的转化率为80% | ||
B、平衡时,容器内压强为原来的
| ||
| C、平衡时,C的浓度为0.5mol/L | ||
| D、A的平均反应速率为0.30mol/(L?min) |
下列说法正确的是( )
| A、同周期元素的第一电离能从左往右越来越大 |
| B、同主族元素从上到下第一电离能越来越大 |
| C、同周期元素的电负性从左往右越来越大 |
| D、同主族元素从上到下电负性越来越大 |
当燃烧镁和某金属组成的合金时,所形成的氧化物的质量为反应前合金质量的2倍,则另一种金属可能是( )
| A、铜 | B、钠 | C、铍 | D、铝 |
下列各组结构和性质对比正确的是( )
| A、第一电离能Li<Na |
| B、电负性O<N |
| C、粒子半径F->Mg2+ |
| D、酸性H2SO3>HNO3 |
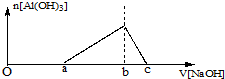 25℃时,向浓度均为0.1mol.L-1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液,表示生成Al(OH)3的物质的量与加入的NaOH溶液的体积的关系如图所示(已知当离子浓度小于1×10-5mol.L-1时为沉淀完全).则下列说法与判断合理的是( )
25℃时,向浓度均为0.1mol.L-1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液,表示生成Al(OH)3的物质的量与加入的NaOH溶液的体积的关系如图所示(已知当离子浓度小于1×10-5mol.L-1时为沉淀完全).则下列说法与判断合理的是( )| A、25℃时,Fe(OH)3的溶解度大于Al(OH)3的溶解度 |
| B、25℃时,Fe(OH)3的溶度积大于Al(OH)3的溶度积 |
| C、当生成的Al(OH)3恰好完全溶解时,溶液中的溶质只有NaAlO2 |
| D、图中2a=b=6(c-b) |
CuCO3和Cu2(OH)2CO3的混合物34.6g,可恰好完全溶解于300mL、2mol?L-1的盐酸中,若加热分解等量的这种混合物可得CuO固体质量为( )
| A、16.0g |
| B、19.2g |
| C、24.0g |
| D、30.6g |
下列各项中的两种物质无论以何种比例混合,只要混合物的总物质的量一定.则完全燃烧时生成水的质量和消耗O2的质量均不变的是( )
| A、C3H6、C3H8O |
| B、C3H6、C2H6O |
| C、C2H2、C6H6 |
| D、CH4、C2H4O2 |
2mol A与2mol B混合于2L的密闭容器中,发生如下反应:2A(g)+3B(g)?2C(g)+zD(g),若2s后,A的转化率为50%,测得v(D)=0.25mol?L-1?s-1,下列推断正确的是( )
| A、v(B)=0.75 mol?L-1?s-1 |
| B、z=2 |
| C、B的转化率为25% |
| D、C的体积分数约为28.6% |