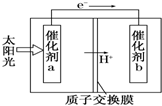
 人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )| A、催化剂b表面的反应是CO2+2H++2e-═HCOOH |
| B、催化剂a表面发生氧化反应,有O2产生 |
| C、催化剂a附近酸性减弱,催化剂b附近酸性增强 |
| D、该过程是将太阳能转化为化学能的过程 |
 人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )| A、催化剂b表面的反应是CO2+2H++2e-═HCOOH |
| B、催化剂a表面发生氧化反应,有O2产生 |
| C、催化剂a附近酸性减弱,催化剂b附近酸性增强 |
| D、该过程是将太阳能转化为化学能的过程 |