甲酸的下列性质中,可以证明它是弱电解质的是( )
| A、1mol/L甲酸溶液的c(H+)=10-2mol/L |
| B、甲酸以任何比与水互溶 |
| C、10mL1mol/L甲酸恰好与10mL1mol/LNaOH溶液完全反应 |
| D、甲酸溶液的导电性比盐酸溶液弱 |
相对分子质量为72的烷烃,其同分异构体有( )种.
| A、3 | B、4 | C、5 | D、6 |
醋酸溶液中存在电离平衡CH3COOH?H++CH3COO-,下列叙述不正确的是( )
| A、醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) |
| B、0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)减小 |
| C、CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动 |
| D、常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7 |
用水稀释0.1mol/L氨水时,溶液中随水量的增加而减小的是( )
A、
| ||
B、
| ||
| C、c(H+)×c(OH-) | ||
| D、n(OH-) |
下列有关同分异构体数目的叙述中,不正确的是( )
| A、1-氯-1-丙烯可以形成顺反异构 |
B、与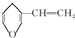 互为同分异构体的芳香族化合物有6种 互为同分异构体的芳香族化合物有6种 |
C、剧毒物质二恶英,其结构为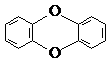 ,已知它的二氯代物有10种同分异构体,则其六氯代物的同分异构体也有10种 ,已知它的二氯代物有10种同分异构体,则其六氯代物的同分异构体也有10种 |
| D、C11H16的苯的同系物中,经分析分子中除苯环外不含其他环状结构,还含有两个-CH3、两个-CH2-、一个-CH-,它的可能结构有4种 |
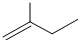
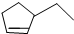
同分异构现象是造成有机物种类繁多的重要原因之一.下列物质不是1-戊烯(CH2=CH-CH2-CH2-CH3)的同分异构体的是( )
| A、CH3-CH=CH-CH2-CH3 |
B、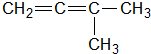 |
C、 |
D、 |
 此烃名称为
此烃名称为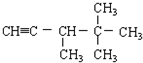 可命名为
可命名为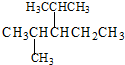 的烃可命名为:
的烃可命名为:
 醋酸是一种常见的弱酸.
醋酸是一种常见的弱酸.



