由锌、铁、铝、镁四种金属中的两种组成的合金10g,与足量的盐酸反应产生的氢气在标准状况下为11.2L,则此合金可能是( )
| A、锌 镁 |
| B、铁 铝 |
| C、铁 锌 |
| D、镁 铁 |
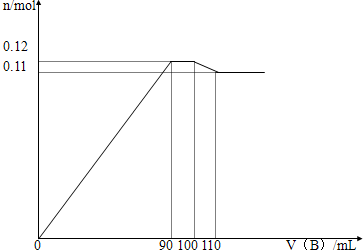
钠-钾合金可在核反应堆中用作热交换液.5.05g钠-钾合金溶于200mL水生成0.075mol氢气.
(1)计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化).
(2)计算并确定该钠-钾合金的化学式.
(1)计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化).
(2)计算并确定该钠-钾合金的化学式.
两种有机物以一定比例混合,一定条件下在aL O2(足量)中燃烧,充分反应后恢复到原状态,再通过足量Na2O2层,得到气体仍是aL,下列混合有机物中符合此条件的是( )
| A、CH4 C2H4 |
| B、CH3OH CH3COOH |
| C、C2H6 HCHO |
| D、HCHO CH3COOCH3 |
将可能混有下列物质的硫酸铵样品13.2g,在加热条件与过量氢氧化钠溶液反应,可收集到气体4.3L (标准状况),则该样品内不可能含有的物质是( )
| A、碳酸氢铵和硝酸铵 |
| B、碳酸铵和硝酸铵 |
| C、氯化铵和碳酸氢铵 |
| D、氯化铵和碳酸铵 |
在50mL FeCl3和CuCl2的混合溶液中,FeCl3和CuCl2的浓度均为1mol?L-1.在此混合液中加入100mL NaOH溶液,恰好完全反应,则该NaOH溶液的浓度为( )
| A、0.5 mol?L-1 |
| B、1 mol?L-1 |
| C、1.25 mol?L-1 |
| D、2.5 mol?L-1 |
7.6克铜镁合金完全溶解于250mL密度为1.4g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体5.6L(标准状况),向反应后的溶液中加入1.0mol/L的KOH溶液,当金属离子全部沉淀时,得到12.7克沉淀.下列说法不正确的是( )
| A、该浓硝酸的物质的量浓度是14.0mol/L |
| B、得到12.7克沉淀时,加入的KOH溶液的体积是3.2L |
| C、该合金中铜与镁的物质的量之比是1:2 |
| D、NO2和N2O4的混合气体中,N2O4的体积分数是20% |
300℃时,将100mL由H2O、CO2和N2组成的混合气体,通入到盛有足量Na2O2的密闭容器中(容器体积保持不变),充分反应后恢复到原温度时,容器内的压强变为原来的四分之三.则原混合气体中N2的体积分数为( )
| A、33.3% | B、25% |
| C、50% | D、75% |
 大多金属碳化物能与水剧烈反应,生成相应氢氧化物和气态烃,如:
大多金属碳化物能与水剧烈反应,生成相应氢氧化物和气态烃,如: