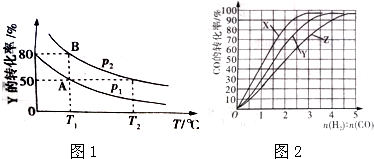
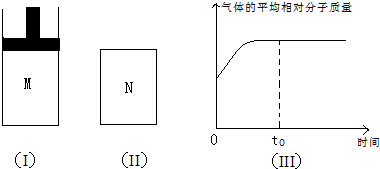
氨水有下列平衡NH3.H2O?NH4++OH-,当其它条件不变时,改变下列条件,平衡向左移,且c(NH4+)增大的是( )
| A、加NaOH |
| B、加盐酸 |
| C、加NH4Cl |
| D、加同浓度氨水 |
有一瘦身用的非天然油脂,其结构如下,下列说法正确的是( )
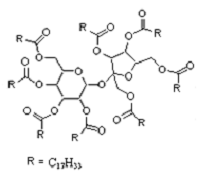

| A、该非天然油脂属于高级脂肪酸的甘油酯 |
| B、该非天然油脂与氢氧化钠溶液共热,其水解产物不与溴水反应 |
| C、该非天然油脂为高分子化合物 |
| D、该非天然油脂在稀硫酸的作用下水解最终生成三种有机化合物 |
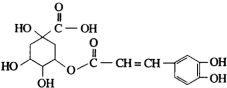 金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法正确的是( )
金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法正确的是( )| A、绿原酸的分子式为C16H8O9 |
| B、1mol绿原酸最多与7molNaOH反应 |
| C、1个绿原酸分子中含有4个手性碳原子 |
| D、绿原酸分子中有4种化学环境不同的氢原子 |